Формула сахарозы
Определение и формула сахарозы
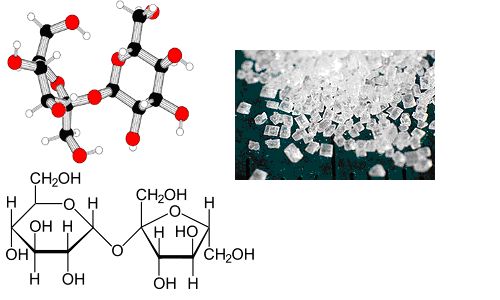
Формула – ![]()
Молярная масса равна ![]() г/моль.
г/моль.
Физические свойства – бесцветные кристаллы, хорошо растворяется в воде.
Является невосстанавливающим сахаром.
Широко распространенное резервное вещество растений, образующееся при фотосинтезе.
При нагревании выше температуры плавления сахароза разлагается с изменением окраски расплава.
Химические свойства сахарозы
- Сахароза подвергается гидролизу. Для этого кипятят раствор сахарозы в кислой среде, а затем нейтрализуют кислоту щелочью. После этого нагревают раствор. При этом появляются соединения с альдегидными группами (глюкоза и фруктоза), которые и восстанавливают
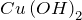 до
до 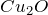 :
:
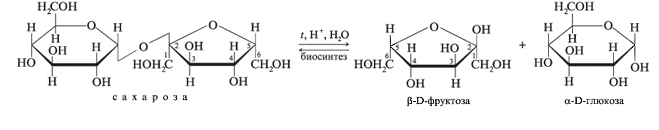
Получение
Сахарозу преимущественно получают из сока сахарного тростника или сахарной свеклы. Ее химический синтез достаточно сложный и трудоемкий, поэтому не представляет практического интереса.
Применение
Сахароза находит многочисленное применение и в первую очередь как пищевой продукт — сахар. Она также служит в качестве исходного вещества в различных ферментационных процессах получения этилового спирта, глицерина, лимонной кислоты. Применяется также для изготовления лекарств.
Качественная реакция
Качественной реакцией на сахарозу является взаимодействие с гидроксидом меди (II). За счет наличия в молекуле сахарозы нескольких гидроксильных групп происходит взаимодействие аналогично глицерину и глюкозе. Если добавить раствор ![]() к осадку
к осадку ![]() он растворится и жидкость окрашивается в синий цвет.
он растворится и жидкость окрашивается в синий цвет.
Примеры решения задач
| Задание | Рассчитайте молярную массу сахарозы, если известно, что ее раствор с массовой долей |
| Решение | Запишем выражение для осмотического давления Комбинируя эти два уравнения выразим молярную массу: Плотность раствора сахарозы с массовой долей Осмотическое давление переведем в Паскали: Абсолютная температура равна: |
| Ответ |
| Задание | Сколько выделится теплоты при сгорании |
| Решение | Запишем уравнение химической реакции горения сахарозы:
Из справочника находим стандартную энтальпию сгорания сахарозы, рассчитанную на моль: Рассчитаем количество моль сахарозы: Вычислим |
| Ответ | Выделится |











