Формула бромида аммония
Определение и формула бромида аммония

Формула – ![]()
Молярная масса равна ![]() г/моль.
г/моль.
Физические свойства – бесцветное или белое кристаллическое вещество.
При нагревании сублимируется и подвергается разложению.
Достаточно устойчивый на свету и на воздухе, если отсутствуют примесные соединения.
Химические свойства бромида аммония
- Разлагается при температуре выше
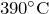 . Процесс протекает по уравнению:
. Процесс протекает по уравнению:
![Rendered by QuickLaTeX.com \[ NH_4Br =NH_3+HBr \]](http://ru.solverbook.com/wp-content/ql-cache/quicklatex.com-63d97e61479b969d0a94ff7350e1ba6e_l3.png)
- Данная соль реагирует с кислотами:
![Rendered by QuickLaTeX.com \[ 2NH_4Br + H_2SO_4 = \left ( NH_4 \right )_2SO_4 + 2HBr \uparrow \]](http://ru.solverbook.com/wp-content/ql-cache/quicklatex.com-ba1c8ba2fcfd7464c3b783d7a2819366_l3.png)
- Вступает в химическое взаимодействие с щелочами:
![Rendered by QuickLaTeX.com \[ NH_4Br + NaOH=NaBr+NH_3 \uparrow +H_2O \]](http://ru.solverbook.com/wp-content/ql-cache/quicklatex.com-c054e9b907aeed84ab0b4f7cab2807e7_l3.png)
- Может принимать участие в окислительно-восстановительных реакциях:
![Rendered by QuickLaTeX.com \[ 2NH_4Br + Mg=MgBr_2 +H_2 \uparrow +2NH_3 \uparrow \]](http://ru.solverbook.com/wp-content/ql-cache/quicklatex.com-c4936726d201f2492c02d4ae6b6fa54f_l3.png)
Получение
Бромид аммония можно получить по реакции аммиака с ![]() :
:
![]()
Применение
Одним из основных способов применения бромида аммония является изготовление лекарств.
Примеры решения задач
| Задание | Сколько литров |
| Решение | Запишем уравнение химической реакции образования бромида аммония:
Определим количество моль
Из стехиометрии реакции следует, что:
Определим объем газов на основании молярного объема
|
| Ответ | |
| Задание | Определите массовую долю бромида аммония в растворе, который имеет осмотическое давление 1 атм при |
| Решение | Бромид аммония — сильный электролит и диссоциирует нацело с образованием двух частиц:
Запишем выражение для определения осмотического давления для сильного электролита: где
Пересчитаем молярную концентрацию в массовую долю, приняв плотность раствора за единицу, так как концентрация мала: Подставим численные значения:
|
| Ответ | |











