Формула метилового спирта
Определение и формула метилового спирта
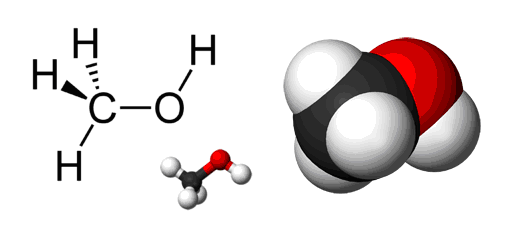
Формула – ![]()
Молярная масса равна ![]() г/моль.
г/моль.
Физические свойства – бесцветная жидкость со слабым спиртовым запахом.
Метанол чрезвычайно ядовит, кипит при температуре ![]() .
.
Химические свойства метилового спирта
- При взаимодействии метанола с щелочными металлами гидроксильный водород замещается металлом:
![Rendered by QuickLaTeX.com \[ 2CH_3OH+2Na\rightarrow 2CH_3ONa+H_2 \]](http://ru.solverbook.com/wp-content/ql-cache/quicklatex.com-e89d55115de0e94763e1d2057a062ffb_l3.png)
- Метанол реагирует с минеральными и карбоновыми кислотами. При этом образуются сложные эфиры:
![Rendered by QuickLaTeX.com \[ CH_3OH+HOSO_3H \rightleftarrows CH_3OSO_3H+H_2O \]](http://ru.solverbook.com/wp-content/ql-cache/quicklatex.com-febeb0b91b298b708a945ad1888b7f13_l3.png)
![Rendered by QuickLaTeX.com \[ CH_3OH+CH_3COOH\rightleftarrows CH_3COOCH_3+H_2O \]](http://ru.solverbook.com/wp-content/ql-cache/quicklatex.com-381db202c2825a9dbd1dce9ed2e428ad_l3.png)
- Метанол может реагировать с галогенводородными кислотами, галогенидами фосфора:
![Rendered by QuickLaTeX.com \[ CH_3OH+HCl\rightleftarrows CH_3Cl+H_2O \]](http://ru.solverbook.com/wp-content/ql-cache/quicklatex.com-dff1241665830082dcff3b901573a64c_l3.png)
Получение
Метанол можно получать различными методами: сухой перегонкой древесины, разложением солей метановой кислоты при высокой температуре.
Промышленный способ основывается на взаимодействии монооксида углерода и водорода в присутствии медь-цинкового окисного катализатора:
![]()
Применение
Древесный спирт находит широкое применение в органической химии, особенно в качестве растворителя.
Также используется в органическом синтезе при производстве формальдегида.
Применяется как источник энергии.
Ни в коем случае его нельзя применять во внутрь.
Примеры решения задач
| Задание | Рассчитайте теплоту испарения метанола при стандартных условиях. |
| Решение | Запишем уравнение данного процесса:
Теплоту испарения рассчитаем по справочным данным (энтальпиям образования):
|
| Ответ | |
| Задание | Рассчитайте концентрацию ионов |
| Решение | Из справочника возьмем константы диссоциации воды и спирта:
Из этих значений видно, что Это означает, что диссоциация спирта не влияет на равновесные концентрации В свою очередь диссоциация воды сильно влияет на равновесные концентрации Сначала рассмотрим диссоциацию воды: В состоянии равновесия Теперь рассмотрим диссоциацию спирта с учетом диссоциации воды: В состоянии равновесия: Так как Так как Отсюда |
| Ответ | |











