Формула ацетата аммония
Определение и формула ацетата аммония

Формула – ![]()
Молярная масса равна ![]() г/моль.
г/моль.
Физические свойства – бесцветное кристаллическое вещество, хорошо растворимое в воде.
Ацетат аммония – соль, гидролизующаяся и по катиону и по аниону, очень гигроскопичная соль.
Химические свойства ацетата аммония
- Разлагается при достаточно низкой температуре. Образуется ацетамид и
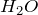 . Процесс протекает по уравнению:
. Процесс протекает по уравнению:
![Rendered by QuickLaTeX.com \[ CH_3COONH_4 \rightarrow CH_3C\left ( O \right )NH_2 + H_2O \]](http://ru.solverbook.com/wp-content/ql-cache/quicklatex.com-d59464b98c51d2f864fd31952fb58935_l3.png)
Получение
Ацетат аммония производится нейтрализацией уксусной кислоты карбонатом аммония или насыщением ледяной уксусной кислоты сухим газообразным аммиаком.
Применение ацетата аммония
Ацетат аммония находит применение в качестве антиобледенителя, буфера, коагулянта, как реагент в органическом синтезе.
Примеры решения задач
| Задание | Рассчитайте константу гидролиза |
| Решение | Данная соль подвергается гидролизу и по катиону и по аниону. Запишем уравнения реакций данного процесса:
Выведем уравнение для вычисления константы гидролиза Подставим численные значения в полученную формулу, тогда: |
| Ответ | |
| Задание | Напишите реакцию гидролиза |
| Решение | Ацетат аммония — соль, образованная слабой кислотой и слабым основанием, поэтому гидролиз протекает и по аниону и по катиону:
Суммарная реакция: Так как при гидролизе образуются ионы |
| Ответ | Реакция среды — нейтральная. |






![Rendered by QuickLaTeX.com \[ K = \frac{\left [ CH_3COOH \right ] \cdot \left [ NH _4OH \right ]}{\left [ CH_3COO^- \right ] \cdot \left [ NH_4^+ \right ]}\cdot \frac{\left [ H^+ \right ]}{\left [ H^+ \right ]} \cdot \frac{\left [ OH^- \right ]}{\left [ OH^- \right ]}= \]](http://ru.solverbook.com/wp-content/ql-cache/quicklatex.com-96a71580e2d4d3177e8052eb4cd14c95_l3.png)
![Rendered by QuickLaTeX.com \[ =\frac{\left [ CH_3COOH \right ] }{\left [ CH_3COO^- \right ] \cdot \left [ H^+ \right ]}\cdot \frac{\left [ NH_4OH \right ]}{\left [ NH_4^+ \right ] \cdot \left [ OH^- \right ]}\cdot \frac{\left [ H^+ \right ] \cdot \left [ OH^- \right ]}{1} = \]](http://ru.solverbook.com/wp-content/ql-cache/quicklatex.com-0489293df2f7877bd7e93b8e27a539b3_l3.png)





