Формула сульфата алюминия
Определение и формула сульфата алюминия

Формула – ![]()
Молярная масса равна ![]() г/моль.
г/моль.
Физические свойства – белое вещество (может иметь разные оттенки), плавящееся с разложением.
В обычных условиях образует кристаллогидрат с формулой ![]() .
.
Химические свойства сульфата алюминия
- Сульфат алюминия хорошо растворяется в воде (происходит гидролиз по катиону):
![Rendered by QuickLaTeX.com \[ Al_2\left ( SO_4 \right )_3 + 12H_2O=2\left [ Al\left ( H_2O \right )_6\right ]^{3+}+3SO_4^{2-} \]](http://ru.solverbook.com/wp-content/ql-cache/quicklatex.com-19dd3209dcc0975de2077f6e31a247ca_l3.png)
![Rendered by QuickLaTeX.com \[ \left [ Al\left ( H_2O \right )_6\right ]^{3+}+H_2O=\left [ Al\left ( H_2O \right )_5\left ( OH \right ) \right ]^{}+H_3O^{+} \]](http://ru.solverbook.com/wp-content/ql-cache/quicklatex.com-da4fba9dd8549d6f9aa7f6272694f3da_l3.png)
- При нагревании до температуры
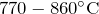 протекает окислительно-восстановительная реакция диспропорционирования (сульфат алюминия разлагается на оксид алюминия, оксид серы
протекает окислительно-восстановительная реакция диспропорционирования (сульфат алюминия разлагается на оксид алюминия, оксид серы 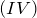 и кислород):
и кислород):
![Rendered by QuickLaTeX.com \[ 2Al_2\left ( SO_4 \right )_3=2Al_2O_3+6SO_2+3O_2 \]](http://ru.solverbook.com/wp-content/ql-cache/quicklatex.com-4daca76e7b4460008ff43f32a3fca1ee_l3.png)
- Реагирует с кипящей водой:
![Rendered by QuickLaTeX.com \[ Al_2\left ( SO_4 \right )_3+6H_2O=2Al\left ( OH \right )_3 \downarrow 3H_2SO_4 \]](http://ru.solverbook.com/wp-content/ql-cache/quicklatex.com-5119487d7851df510ef83c66a9ba8299_l3.png)
- Взаимодействует с растворами разбавленных щелочей:
![Rendered by QuickLaTeX.com \[ Al_2\left ( SO_4 \right )_3+6NaOH=2Al\left ( OH \right )_3 \downarrow +3Na_2SO_4 \]](http://ru.solverbook.com/wp-content/ql-cache/quicklatex.com-aa772d2d84de5bcf903bc12730da7928_l3.png)
- Вступает в реакцию с растворами концентрированных щелочей:
![Rendered by QuickLaTeX.com \[ Al_2\left ( SO_4 \right )_3+8NaOH=2Na\left [ Al\left ( OH \right )_4 \right ]+3Na_2SO_4 \]](http://ru.solverbook.com/wp-content/ql-cache/quicklatex.com-eb8199b71e15bcbeba8440720746b48e_l3.png)
- Реагирует с гидроксидом аммония:
![Rendered by QuickLaTeX.com \[ Al_2\left ( SO_4 \right )_3+6NH_4OH=2Al\left ( OH \right )_3 \downarrow +3\left ( NH_4 \right )_2SO_4 \]](http://ru.solverbook.com/wp-content/ql-cache/quicklatex.com-ed0fca1e99227814c7fd8d19998f9993_l3.png)
- Вступает в реакцию обмена с солями с образованием осадков:
![Rendered by QuickLaTeX.com \[ Al_2\left ( SO_4 \right )_3+3Ba\left ( NO_3 \right )_2=3BaSO_4 \downarrow +2Al\left ( NO_3 \right )_3 \]](http://ru.solverbook.com/wp-content/ql-cache/quicklatex.com-f09aae4b90bb5ac6c2328c92b0bf228c_l3.png)
Получение
Сульфат алюминия можно получить при взаимодействии оксида алюминия с кислым сульфатом калия при высокой температуре (![]() ):
):
![]()
Применение
Сульфат алюминия находит применение в качестве коагулянта для очистки воды хозяйственно-питьевого и промышленного назначения. Он также применяется во многих отраслях промышленности, например, в бумажной. Кроме того, используется как пищевая добавка ![]() .
.
Примеры решения задач
| Задание | Качественно определите |
| Решение | Данная соль образована слабым основанием и сильной кислотой, поэтому гидролиз протекает по катиону:
В результате гидролиза образуется ион Запишем общую реакцию гидролиза: |
| Ответ |
| Задание | Рассчитайте массу |
| Решение | Определим количество моль кристаллогидрата:
Из 1 моль кристаллогидрата получается 1 моль соли, тогда:
Определим массу сульфата алюминия:
|
| Ответ |











