Формула воды
Химическая и структурная формула воды
Химическая формула: Н2O
Структурная формула:
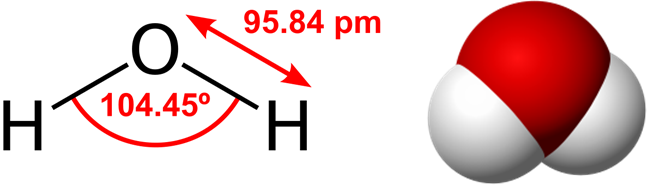
Молярная масса: 18,01528 г/моль.
Альтернативные названия: оксид водорода, гидроксид водорода, гидроксильная кислота, монооксид дигидрогена, оксидан, дигидромонооксид.
В молекуле воды атом кислорода находится в состоянии sp3–гибридизации, поскольку в образовании гибридных орбиталей участвуют не только валентные электроны, но и неподеленные электронные пары. Гибридные орбитали направлены к вершинам тетраэдра:
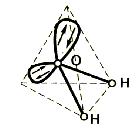
Вследствие большой разницы электроотрицательностей кислорода и водорода связи в молекуле сильно поляризованы, и происходит смещение электрон ной плотности в сторону кислорода. Молекула воды обладает большим дипольным моментом, поскольку полярные связи расположены несимметрично.
С сильной поляризацией связи О – Н связано образование водородных связей между молекулами воды. Каждая молекула воды может образовывать до четырёх водородных связей – две из них образует атом кислорода, а еще две – атомы водорода:
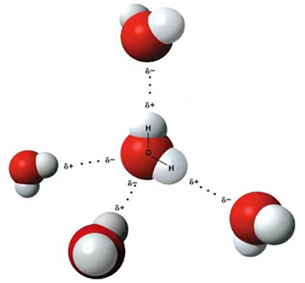
Образование водородных связей определяет более высокую температуру кипения, вязкость и поверхностное натяжение воды по сравнению с гидридами аналогов (серы селена и теллура).
Изотопные модификации воды
В зависимости от типа изотопов водорода, входящих в состав молекулы, выделяют следующие изотопные модификации воды:
| Название | Формула |
|---|---|
|
Легкая вода (основной компонент природной воды) |
H2O |
|
Тяжёлая вода (дейтериевая) |
D2O |
|
Сверхтяжёлая вода (тритиевая) |
T2O |
|
Тритий-дейтериевая вода |
TDO |
|
Тритий-протиевая вода |
THO |
|
Дейтерий-протиевая вода |
DHO |
С учетом того, что у кислорода три стабильных изотопа (16O, 17O и 18O), можно составить 18 формул молекул воды, различающихся изотопным составом. Как правило, природная вода содержит все эти разновидности молекул.
Примеры решения задач по теме «формула воды»
| Задание | В радиатор автомобиля залили 9 л воды и добавили 2 л метилового спирта с плотностью 0,8 г/мл. При какой минимальной температуре можно теперь оставить автомобиль на открытом воздухе, не опасаясь, что вода в радиаторе замерзнет (криоскопическая константа воды равна 1,86 К • кг/моль)? |
| Решение | По закону Рауля понижение температуры кристаллизации разбавленных растворов неэлектролитов равно:

где: Масса метилового спирта равна:
Масса воды равна:
Молярная масса метилового спирта равна 32г/моль Рассчитаем изменение температуры замерзания: 
|
| Ответ | Автомобиль можно оставлять на улице при температуре выше –10,3°С |
| Задание | Сколько граммов Na2SO4 • 10H2O следует растворить в 250 г воды для получения раствора, содержащего 5% безводной соли? |
| Решение | Молярная масса Na2SO4 равна:
Молярная масса кристаллогидрата:
Обозначим количество (моль) растворенной соли как х. Тогда масса раствора будет равна: Масса безводной соли в готовом растворе будет равна: Массовая доля сульфата натрия в растворе: 
Отсюда х будет равен:
Масса кристаллогидрата будет равна:
|
| Ответ | Масса |











