Формула нитрата серебра
Определение и формула нитрата серебра

Химическая формула – ![]()
Молярная масса равна ![]() г/моль.
г/моль.
Физические свойства – это твёрдое вещество, представляющее из себя бесцветные ромбические кристаллы, с плотностью 4,352 г/см![]() , хорошо растворяется в воде 222,5 г/100 г (
, хорошо растворяется в воде 222,5 г/100 г (![]() ).
).
Растворимость в метаноле и этаноле равно соответственно 3,6 г/100 г и 2,12 г/100, температура плавления ![]() , выше
, выше ![]() разлагается.
разлагается.
Химические свойства нитрата серебра
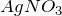 взаимодействует c металлами, стоящими в ряду напряжения левее серебра:
взаимодействует c металлами, стоящими в ряду напряжения левее серебра:
![Rendered by QuickLaTeX.com \[ 2AgNO_3 + Fe = Fe(NO_3)_2 + 2Ag \downarrow \]](http://ru.solverbook.com/wp-content/ql-cache/quicklatex.com-621231e771a01f904b53ca77164834a8_l3.png)
- Взаимодействует с основаниями:
![Rendered by QuickLaTeX.com \[ AgNO_3 + NaOH = Ag_2O \downarrow + H_2O + NaNO_3 \]](http://ru.solverbook.com/wp-content/ql-cache/quicklatex.com-b8868981c43ada8c0a1e3edda5c053fd_l3.png)
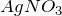 взаимодействует кислотами и солями по обменному механизму с выпадением осадка или комплексообразованием, с органическими веществами, которые имеют в своём составе альдегидную группу:
взаимодействует кислотами и солями по обменному механизму с выпадением осадка или комплексообразованием, с органическими веществами, которые имеют в своём составе альдегидную группу:
![Rendered by QuickLaTeX.com \[ AgNO_3 + HCl = AgCl \downarrow + HNO_3 \]](http://ru.solverbook.com/wp-content/ql-cache/quicklatex.com-d5a418e6be4f6c279e7c91e40cf696b2_l3.png)
![Rendered by QuickLaTeX.com \[ AgNO_3 + NaCl = AgCl \downarrow + NaNO_3 \]](http://ru.solverbook.com/wp-content/ql-cache/quicklatex.com-0af99e329a8f5d600378d70809b537a6_l3.png)
![Rendered by QuickLaTeX.com \[ AgNO_3 + KCN = AgCN \downarrow + KNO_3 \]](http://ru.solverbook.com/wp-content/ql-cache/quicklatex.com-f08ef1fe789e13500daa0fc1c6698e52_l3.png)
![Rendered by QuickLaTeX.com \[ AgNO_3 + 2KCN = K[Ag(CN)_2] + KNO_3 \]](http://ru.solverbook.com/wp-content/ql-cache/quicklatex.com-f29c9297ad07b1447e0ebc5fcb201d72_l3.png)
![Rendered by QuickLaTeX.com \[ 2AgNO_3 + 3NH_4OH + HCHO = 2Ag \downarrow + HCOONH_4 + 2NH_4NO_3 + 2H_2O \]](http://ru.solverbook.com/wp-content/ql-cache/quicklatex.com-f9ac6ca2b10e1243d14ac645c2b9b3b6_l3.png)
- При нагревании
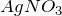 разлагается:
разлагается:
![Rendered by QuickLaTeX.com \[ 2AgNO_3 = 2Ag + 2NO_2 \uparrow + O_2 \uparrow \]](http://ru.solverbook.com/wp-content/ql-cache/quicklatex.com-a06f98a22bc05da0bb77f95e2e506026_l3.png)
Получение
Нитрат серебра получают растворением металлического серебра в концентрированной азотной кислоте:
![]()
Качественная реакция
Качественной реакцией на нитрат-ион является образование тёмно-бурого раствора сульфата нитрозожелеза (II) при взаимодействии ![]()
![]()
![]()
Применение
Нитрат серебра применяется в медицине для прижигания небольших ран и бородавок.
В малых концентрациях он используется в качестве противовоспалительного и вяжущего средства.
Также используется в изготовлении зеркал.
Примеры решения задач
| Задание | Рассчитайте эффективную степень диссоциации |
| Решение | На первом шаге вычислим изотонический коэффициент, который показывает формальное число частиц, на которое продиссоциировало соединение:
Рассчитаем степень диссоциации |
| Ответ |
| Задание | Рассчитайте концентрацию ионов серебра |
| Решение | Равновесные концентрации частиц: Здесь |
| Ответ |











