Формула ацетона
Определение и формула ацетона
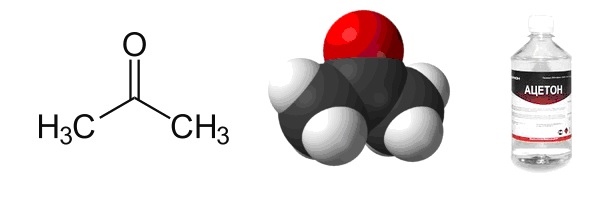
Химическая формула – ![]()
Молярная масса равна ![]() г/моль.
г/моль.
Физические свойства – это прозрачная подвижная жидкость с характерным резким запахом, достаточно летучая. С водой, низшими спиртами и эфирами смешивается неограниченно. Температура плавления и кипения равны соответственно ![]() и
и ![]() , плотность при комнатной температуре 0,7899 г/см
, плотность при комнатной температуре 0,7899 г/см![]() .
.
Химические свойства ацетона
Ацетон, являясь кетоном, взаимодействует с атомарным водородом в момент его выделения с образованием пинакона, с синильной кислотой с образованием ![]() -оксинитрила, с гидросульфитом натрия с образованием гидросульфитного производного ацетона, с гидроксиламином с образованием ацетоноксима, с гидразином с образованием гидразона и азима, со спиртами с образованием полуацеталя и ацеталя, с бромом и йодом с замещением атома водорода на атом галогена, с самим собой в реакциях конденсации в щелочной среде с образованием
-оксинитрила, с гидросульфитом натрия с образованием гидросульфитного производного ацетона, с гидроксиламином с образованием ацетоноксима, с гидразином с образованием гидразона и азима, со спиртами с образованием полуацеталя и ацеталя, с бромом и йодом с замещением атома водорода на атом галогена, с самим собой в реакциях конденсации в щелочной среде с образованием ![]() -кетоноспирта и далее непредельного кетона. Приведём некоторые реакции:
-кетоноспирта и далее непредельного кетона. Приведём некоторые реакции:
- Взаимодействие с гидросульфитом натрия:
![Rendered by QuickLaTeX.com \[ (CH_3)_2CO + NaHSO_3 \rightarrow (CH_3)_2C(OH)SO_3Na \]](http://ru.solverbook.com/wp-content/ql-cache/quicklatex.com-2ba892844a9ea64d9d75b90bb23c3f79_l3.png)
- Альдольная конденсация:
![Rendered by QuickLaTeX.com \[ 2(CH_3)_2CO \rightarrow (CH_3)_2C(OH)CH_2C(O)CH_3 \]](http://ru.solverbook.com/wp-content/ql-cache/quicklatex.com-5e2187c38fc6e11a3a733caa8467a771_l3.png)
- Взаимодействие с синильной кислотой:
![Rendered by QuickLaTeX.com \[ (CH_3)_2CO + HCN \rightarrow (CH_3)_2C(OH)CN \]](http://ru.solverbook.com/wp-content/ql-cache/quicklatex.com-b2414e0c52c80907432124cc9ba957b1_l3.png)
Получение
Ацетон получают окислением изопропанола кислородом при ![]() с катализатором (медь, серебро, платина, никель):
с катализатором (медь, серебро, платина, никель):
![]()
Также ацетон получают окислением пропена:
![]()
Качественная реакция
Качественной реакцией на ацетон является интенсивно-красное окрашивание при взаимодействии нитропруссидом натрия в щелочной среде:
![]()
Применение
Ацетон имеет широкое применение как прекурсор для синтеза многих важных веществ (уксусный ангидрид, кетен, окись мезитила, метилизобутилкетон, метилметакрилат, дифенилпропан и так далее). Также применяется как растворитель, для мытья и быстрой сушки лабораторной посуды.
Примеры решения задач
| Задание | Смешали |
| Решение | Определим число моль и мольные доли компонентов раствора:
Вычислим давление пара каждого компонента над раствором и общее давление: Рассчитаем мольные доли компонентов паре: |
| Ответ |
| Задание | Рассчитайте активность и коэффициент активности ацетона в водном растворе, если мольная доля ацетона равна |
| Решение | Рассчитаем активность ацетона:
Определим коэффициент активности: |
| Ответ |











