Этаналь
Характеристики и физические свойства этаналя
Он хорошо растворим в воде, спирте и эфире.
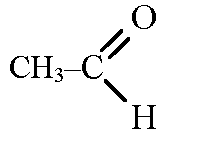
Рис. 1. Строение молекулы этаналя.
Таблица 1. Физические свойства этаналя.
|
Молекулярная формула |
CH3-C(O)H |
|
Молярная масса |
44 |
|
Плотность (0oС), г/см3 |
0,784 |
|
Температура плавления, oС |
-123,37 |
|
Температура кипения, oС |
20,2 |
Получение этаналя
Наиболее популярным способом получения этаналя является окисление этанола:
CH3-CH2-OH + [O] →CH3-C(O)H.
Кроме этого используются и другие реакции:
- гидролиз 1,1-дигалогеналканов
CH3-CHCl2 + 2NaOHaq→CH3-C(O)-H + 2NaCl + H2O (to).
- пиролиз кальциевый (бариевых) солей карбоновых кислот:
H-C(O)-O-Ca-O-C(O)-CH3→ CH3-C(O)-H + CaCO3 (to).
- гидратация ацетилена и его гомологов (реакция Кучерова)
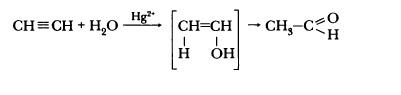
- каталитическое окисление ацетилена
2CH2=CH2 + [O] → 2CH3-C(O)-H (kat = CuCl2, PdCl2).
Химические свойства этаналя
Типичные реакции, характерные для этаналя – реакции нуклеофильного присоединения. Все они протекают преимущественно с расщеплением:
- p-связи в карбонильной группе
— гидрирование
CH3-C(O)-H + H2→ CH3-CH2-OH (kat = Ni).
— присоединение спиртов
CH3-C(O)-H + C2H5OH↔ CH3-CH2-C(OH)H-O-C2H5 (H+).
— присоединение синильной кислоты
CH3-C(O)-H + H-C≡N→CH3-C(CN)H-OH (OH—).
— присоединение гидросульфита натрия
CH3-C(O)-H + NaHSO3→CH3-C(OH)H-SO3Na↓.
- связи С-Н в карбонильной группе
— окисление аммиачным раствором оксида серебра (реакция «серебряного зеркала») – качественная реакция
CH3-(O)H + 2[Ag(NH3)2]OH → CH3-C(O)-ONH4 + 2Ag↓ + 3NH3 + H2O
или упрощенно
CH3-(O)H + Ag2O → CH3-COOH + 2Ag↓ (NH3 (aq)).
— окисление гидроксидом меди (II)
CH3-(O)H + 2Cu(OH)2→ CH3-COOH + Cu2O↓ + 2H2O (OH—, to).
- связи Сα-Н
— галогенирование
CH3-(O)H + Cl2→ CH2Cl-C(O)-H + HCl.
Применение этаналя
Этаналь используется в основном для производства уксусной кислоты и в качестве исходного сырья для синтеза многих органических соединений. Кроме этого этаналь и его производные идут на изготовление некоторых лекарств.
Примеры решения задач
| Задание | Эквимолекулярная смесь ацетилена и этаналя полностью реагирует с 69,6 г Ag2O, растворенного в аммиаке. Определите состав исходной смеси. |
| Решение | Запишем уравнения реакций, указанных в условии задачи:
HC≡CH + Ag2O → AgC≡Cag + H2O (1); H3С-C(O)H + Ag2O →CH3COOH + 2Ag (2). Рассчитаем количество вещества оксида серебра (I): n = m / M; n(Ag2O) = m(Ag2O) / M(Ag2O); M(Ag2O) = 232 г/моль; n(Ag2O) = 69,6 / 232 = 2,6 моль. По уравнению (2) количество вещества этаналя будет равно 0,15 моль. По условию задачи смесь эквимолекулярна, следовательно, ацетилена тоже будет 0,15 моль. Найдем массы веществ, составляющих смесь: M(HC≡CH) = 26 г/моль; M(H3С-C(O)H) = 44 г/моль; m(HC≡CH) = 0,15× 26 = 3,9 г; m(H3С-C(O)H) = 0,15×44 = 6,6 г. |
| Ответ | Масса ацетилена равна 3,9 г, этаналя – 6,6 г. |
| Задание | При каталитическом гидрировании 55 г этаналя образовалась карбоновая кислота. Рассчитайте какая масса кислоты была получена. |
| Решение | Запишем уравнение реакции каталитического окисления этаналя:
CH3-C(O)H + [O] → CH3-COOH. Вычислим количество вещества этаналя (молярная масса равна 44 г/моль): n = m/ M; n(CH3-C(O)H) = m(CH3-C(O)H) / M(CH3-C(O)H); n(CH3-C(O)H) = 55 / 44 = 1,25 моль. Согласно уравнению реакции n(CH3-C(O)H) : n(CH3-COOH) = 1:1, т.е. n(CH3-COOH) = n(CH3-C(O)H) = 1,25 моль. Тогда масса уксусной кислоты будет равна (молярная масса – 60 г/моль): m = n × M; m(CH3-COOH) =1,25 × 60 = 75 г. |
| Ответ | Масса уксусной кислоты равна 75 г. |











