Валентность мышьяка
Общие сведения о валентности мышьяка
Мышьяк существует в виде нескольких аллотропных модификаций. Наиболее устойчив при обычных условиях металлический (серый) мышьяк. Он образует серо-стальную хрупкую кристаллическую массу с металлическим блеском на свежем изломе. Плотность 5,72 г/см3. При нагревании под нормальным давлением серый мышьяк сублимируется. Обладает металлической электрической проводимостью.
При быстром охлаждении пара, состоящего из молекул As4, образуется неметаллическая модификация желтый мышьяк. Плотность 2,0 г/см3. При действии света или слабом нагревании переходит в серый мышьяк.
Валентность мышьяка в соединениях
Мышьяк – тридцать третий по счету элемент Периодической таблицы Д.И. Менделеева. Он находится в четвертом периоде в VA группе. В ядре атома мышьяка содержится 33 протона и 42 нейтрона (массовое число равно 75). В атоме мышьяка есть четыре энергетических уровня, на которых находятся 33 электрона (рис. 1).
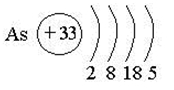
Рис. 1. Строение атома мышьяка.
Электронная формула атома мышьяка в основном состоянии имеет следующий вид:
1s22s22p63s23p63d104s24p3.
А энергетическая диаграмма (строится только для электронов внешнего энергетического уровня, которые по-другому называют валентными):
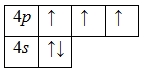
Наличие трех неспаренных электронов свидетельствует о том, что мышьяк способен проявлять валентность III (низшая валентность) в своих соединениях (As2O3, AsH3, HAsO2, H3AsO3).
Для атома мышьяка характерно наличие возбужденного состояния из-за того, что орбитали 4d-подуровня являются вакантными (на четвертом энергетическом слое помимо 4s- и 4p-подуровней есть еще и 4d-подуровень). Электроны 4s-подуровня распариваются и занимают свободную орбиталь 4p -подуровня:
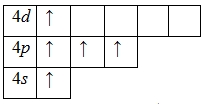
Наличие пяти неспаренных электронов в возбужденном состоянии свидетельствует о том, что мышьяк также проявляет в своих соединениях валентность V (H3AsO4, As2O5) (высшая валентность).
Примеры решения задач
| Задание | Мышьяк образует два оксида. Массовая доля мышьяка в них равна 65,2% и 75,7%. Определите эквивалентные массы мышьяка в обоих оксидах. |
| Решение | Примем массу каждого оксида мышьяка за 100 г. Поскольку содержание мышьяка указано в массовых процентах, то в составе первого оксида находится 65,2 г мышьяка и 34,8 г кислорода (100 – 65,2 = 34,8); в 100 г второго оксида на мышьяк приходится 75,7 г, а на кислород – 24,3 г (100 – 75,7 = 24,3).
Эквивалентная масса кислорода равна 8. Применим закон эквивалентов для первого оксида: m (As) / m(O) = Meq (As) / Meq (O); Meq (As) = m (As) / m(O) × Meq (O); Meq (As) = 65,2 / 34,8 × 8 = 15 г/моль. Расчет для второго оксида проводим аналогично: m (As) / m(O) = Meq (As) / Meq (O); Meq (As) = m (As) / m(O) × Meq (O); Meq (As) = 75,7 / 24,3 × 8 = 25 г/моль. |
| Ответ | Эквивалентные массы мышьяка в оксидах равны 15 г/моль и 25 г/моль. |
| Задание | Приведите электронно-ионные и молекулярные уравнения реакций мышьяка: а) с хлорноватистой кислотой; б) с расплавом гидроксида натрия. |
| Ответ | а) Молекулярное уравнение:
As + HClO = H3AsO4 + HCl. Электронно-ионные уравнения: Aso -3e → As3+; Cl+ + 2e→ Cl— (). б) Молекулярное уравнение: 2As + 4NaOH = NaAsO2 + Na3As + 2H2O. Электронно-ионные уравнения: Aso -3e → As3+; Aso +3e →As3-. |











