Валентность кальция
Общие сведения о валентности кальция
В виде простого вещества кальций представляет собой серебристо-белый металл. На воздухе он тотчас же покрывается желтоватой пленкой продуктов взаимодействия с составными частями воздуха. Кальций довольно тверд (плотность 1,54 г/см3). Температуры плавления и кипения равны 842oС и 1495oС, соответственно.
Валентность кальция в соединениях
Кальций находится в четвертом периоде во IIA группе Периодической таблицы Д.И. Менделеева. Порядковый номер равен 20. В ядре атома кальция содержится 20 протонов и 20 нейтронов (массовое число равно 40). В атоме кальция есть четыре энергетических уровня, на которых находятся 20 электронов (рис. 1).
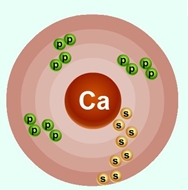
Рис. 1. Строения атома кальция.
Электронная формула атома кальция в основном состоянии имеет следующий вид:
1s22s22p63s23p64s2.
А энергетическая диаграмма (строится только для электронов внешнего энергетического уровня, которые по-другому называют валентными):
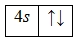
Атом кальция способен переходить в возбужденное состояние: электроны 4s-подуровня распариваются и один из них занимает вакантную орбиталь 4p-подуровня:
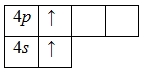
Наличие двух неспаренных электронов свидетельствует о том, что кальций проявляет валентность II в своих соединениях (CaIIO, CaII(OH)2, CaIICl2, CaII(NO3)2 и т.д.). Валентность кальция постоянная.
Примеры решения задач
| Задание | Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
Ca → Ca(OH)2 → CaCO3→Ca(HCO3)2. |
| Ответ | Растворив кальций в воде можно получить мутный раствор соединения известного под названием «известковое молоко» — гидроксида кальция:
Ca+ 2H2O→ Ca(OH)2 + H2↑. Пропустив через раствор гидроксида кальция углекислый газ получаем карбонат кальция: 2Ca(OH)2 + CO2→ CaCO3 + H2O. Добавив к карбонату кальция воды и продолжая пропускать через данную смесь углекислый газ получаем гидрокарбонат кальция: CaCO3+ H2O + CO2→ Ca(HCO3)2. |
| Задание | Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
Ca → CaH2 → Ca(OH)2 → Ca(NO3)2. |
| Ответ | При нагревании кальций вступает в реакцию взаимодействия с водородом с образованием гидрида кальция:
Ca+ H2 → CaH2. При взаимодействии с водой гидрид кальция образует гидроксид кальция: CaH2+ H2O → Ca(OH)2 + 2H2↑. Добавив к раствору гидроксида кальция азотную кислоту можно получить нитрат кальция: Ca(OH)2+ 2HNO3→ Ca(NO3)2 + 2H2O. |











