Молярная масса кальция
Молярная масса кальция
Порядковый номер – 20. Строение атома показано на рис. 1. Металл s-семейства.
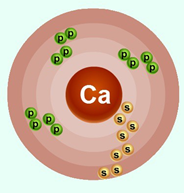
Рис. 1. Схема строения атома кальция.
В обычных условиях кальций представляет собой вещество серебристо-белого цвета. Мягкий, легко режется ножом. На воздухе мгновенно покрывается желтоватой пленкой продуктов взаимодействия с составными частями воздуха. Твердый.
Молярная масса кальция равна 40,078 г/моль. Данное значение показывает отношение массы вещества (m) е число моль данного вещества (n), обозначается M и может быть рассчитано по формуле:
M = m / n.
Иными словами, молярная масса вещества – это масса 1 моль данного вещества, выраженная в г/моль или ккмоль.
Кальций не может существовать в виде газа, только в форме твердого вещества, поэтому для нахождения значения его молярной массы нельзя использовать величину молярного объема или производить расчеты по формуле Менделеева-Клапейрона.
Примеры решения задач
| Задание | Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
Ca → Ca(OH)2 → CaCO3→Ca(HCO3)2. |
| Ответ | Растворив кальций в воде можно получить мутный раствор соединения известного под названием «известковое молоко» — гидроксида кальция:
Ca+ 2H2O→ Ca(OH)2 + H2↑. Пропустив через раствор гидроксида кальция углекислый газ получаем карбонат кальция: 2Ca(OH)2 + CO2→ CaCO3 + H2O. Добавив к карбонату кальция воды и продолжая пропускать через данную смесь углекислый газ получаем гидрокарбонат кальция: CaCO3+ H2O + CO2→ Ca(HCO3)2. |
| Задание | Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
Ca → CaH2 → Ca(OH)2 → Ca(NO3)2. |
| Ответ | При нагревании кальций вступает в реакцию взаимодействия с водородом с образованием гидрида кальция:
Ca+ H2 → CaH2. При взаимодействии с водой гидрид кальция образует гидроксид кальция: CaH2+ H2O → Ca(OH)2 + 2H2↑. Добавив к раствору гидроксида кальция азотную кислоту можно получить нитрат кальция: Ca(OH)2+ 2HNO3→ Ca(NO3)2 + 2H2O. |











