Сахароза
Характеристики и физические свойства сахарозы
Молекула этого вещества построена из остатков α-глюкозы и фруктопиранозы, которые соединяются между собой посредством гликозидного гидроксила (рис. 1).
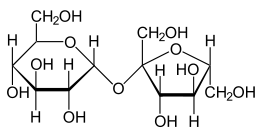
Рис. 1. Структурная формула сахарозы.
Основные характеристики сахарозы приведены в таблице ниже:
|
Молекулярная формула |
C12H22O11 |
|
Молярная масса, г/моль |
342 |
|
Плотность, г/см3 |
1,587 |
|
Температура плавления, oС |
186 |
|
Температура разложения, oF |
367 |
|
Растворимость в воде (25oС), г/100 мл |
211,5 |
Получение сахарозы
Сахароза – важнейший из дисахаридов. Её получают из сахарной свеклы (в ней содержится до 28% сахарозы от сухого вещества) или из сахарного тростника (откуда и происходит название); содержится также в соке березы, клена и некоторых фруктов.
Химические свойства сахарозы
При взаимодействии с водой сахароза гидрозуется. Эта реакция проводится в присутствии кислот или щелочей, а её продуктами являются образующие сахарозу моносахариды, т.е. глюкоза и фруктоза.
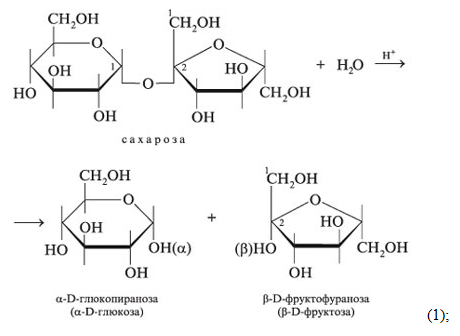
C12H22O11 + H2O → C6H12O6 (глюкоза) + C6H12O6 (фруктоза) (2).
Применение сахарозы
Сахароза нашла свое применение, главным образом, в пищевой индустрии: её используют как самостоятельный продукт питания, а также в качестве консерванта. Кроме этого данный дисахарид может служит субстратом для получения ряда органических соединений (биохимия), а также составным компонентом многих лекарств (фармакология).
Примеры решения задач
| Задание | В химической лаборатории имеются два раствора, один из который глицерин, а второй сахароза. Какие химические превращения нужно осуществить, чтобы понять в какой пробирке глицерин, а в какой сахароза? |
| Решение | Глицерин – это трехатомный спирт, в составе которого есть три гидроксильные группы. Сахароза – углевод, построенный из остатков глюкозы и фруктозы.
Для того, чтобы определить, где какой раствор, добавим в каждую пробирку несколько капель разбавленного раствора серной или соляной кислоты. Визуально мы не будем наблюдать никаких изменений, однако сахароза будет гидролизоваться: C12H22O11 + H2O → C6H12O6 (глюкоза) + C6H12O6 (фруктоза). Глюкоза – альдо-спирт, поскольку содержит пять гидроксильных и одну карбонильную группу. Поэтому, чтобы отличить её от глицерина проведем качественную реакцию на альдегиды – реакцию «серебряного» зеркала – взаимодействие с аммиачным раствором оксида серебра. В обе пробирки добавим указанный раствор. В случае добавления его к трехатомному спирту мы не будем наблюдать никаких признаков химической реакции. Если же в пробирке есть глюкоза, то будет выделяться коллоидное серебро: C6H12O6 + 2[Ag(NH3)2]OH = C6H12O7 + 2Ag↓ + 2NH3↑ + H2O. |
| Задание | Какую массу сахарозы нужно подвергнуть гидролизу, чтобы на выходе получить 35г глюкозы? |
| Решение | Запишем уравнение реакции гидролиза сахарозы:
C12H22O11 + H2O → C6H12O6 (глюкоза) + C6H12O6 (фруктоза). Найдем количество вещества глюкозы, учитывая условия задачи (молярная масса – 180 г/моль): ν = m/ M; ν (C6H12O6) = m (C6H12O6)/ M (C6H12O6) = 35/180 = 0,2 моль. Согласно уравнению реакции ν (C6H12O6) = ν (C12H22O11) = 0,2 моль. Найдем массу сахарозы, вступившей в реакцию гидролиза (молярная масса – 342г/моль): m= ν× M; m(C6H12O6)= ν(C6H12O6)× M(C6H12O6) = 0,2×342 = 68,4 г. |
| Ответ | Масса сахарозы равна 68,4 г |











