Глицерин
Характеристики и физические свойства глицерина
Его температуры плавления и кипения равны 18oС и 290oС соответственно. Глицерин гигроскопичен, хорошо смешивается с водой и этанолом. Абсолютно чистый безводный глицерин затвердевает при +18oС, но получить его в твердом виде чрезвычайно сложно. Строение молекулы глицерина представлено на рис. 1.
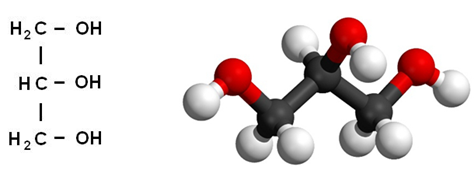
Рис. 1. Строение молекулы глицерина.
Глицерин широко распространен в живой природе. Он играет важную роль в процессах обмена в организмах животных, входит в состав большинства липидов – жиров и других веществ, содержащихся в животных и растительных тканях и выполняющих в живых организмах важнейшие функции.
Получение глицерина
Старейший способ производства глицерина – гидролиз жиров и масел:
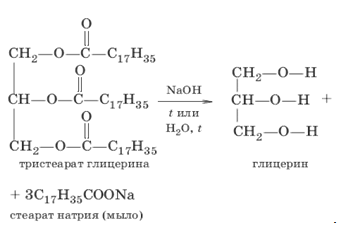
В настоящее время глицерин получают синтетическим путем из пропилена, образующегося при крекинге нефти. При этом используют разные пути превращения пропилена в глицерин. Наиболее перспективный способ – окисление пропилена кислородом воздуха в присутствии катализатора и при высокой температуре (kat = Cu, t0 = 370). Процесс идет в несколько стадий.
Химические свойства глицерина
Глицерин является представителем трехатомных спиртов, для которых, как для гидроксилсодержащих соединений характерны те же реакции, что и для одноатомных спиртов.
Глицерин реагирует с активными металлами (калием, натрием и др.), замещающими водород во всех гидроксильных группах, вступают в реакции с галогеноводородами (HCl, HBr и др.), в реакции дегидратации, образуя различные эфиры.
Глицерин имеет и специфические свойства, отличающие его от одноатомных спиртов: он вступает в реакцию, не только со щелочными металлами, но и с некоторыми основаниями, в том числе нерастворимыми, например с гидроксидом меди (II):
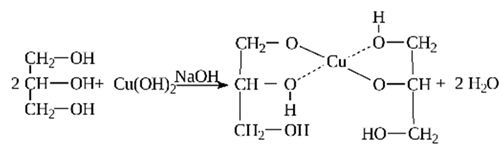
Результатом реакции глицерина с гидроксидом меди (II) является глицерат меди (сложное комплексное соединение ярко-синего цвета). Эта реакция – качественная реакция на многоатомные спирты.
Важнейшей в практическом отношении является реакция нитрования глицерина, в результате которой образуется тринитроглицерин C3H5(ONO2)3:
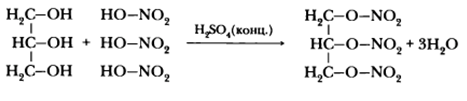
Применение глицерина
Глицерин является компонентом многих пищевых продуктов, кремов и косметических средств.
Примеры решения задач
| Задание | С помощью каких реакций можно осуществить следующие превращения:
Хлорэтан→ Этилен → 1,2-Дибромэтан → Этиленгликоль. |
| Ответ | Получение этилена из хлорэтана можно осуществить по реакции дегалогерирования:
2CH3-CH2-Cl + Zn → 2CH2=CH2 + ZnCl2. Реакция бромирования этилена, протекающая в среде неполярного инертного растворителя (наиболее часто для этой цели используют тетрахлорметан) по механизму электрофильного присоединения позволяет получить 1,2-дибромэтан: CH2=CH2 + Br2→ Br-CH2-CH2-Br. При взаимодействии 1,2-дибромэтана с водным раствором щелочи происходит образование двухатомного спирта этиленгликоля: Br-CH2-CH2-Br + NaOH→ HO-CH2-CH2-OH + 2NaBr. |
| Задание | С помощью каких реакций можно осуществить следующие превращения:
Глицерин → 1,2,3-Трихлорпропан → Глицерин → Нитроглицерин. |
| Ответ | Многоатомные спирты, например, глицерин, способны проявлять основные свойства взаимодействую с соляной кислотой:
HO-CH2-C(OH)H-CH2-OH + 3HCl → Cl-CH2-C(Cl)H-CH2-Cl + 3H2O. При взаимодействии 1,2,3-трихлорпропана с водным раствором щелочи происходит образование трехатомного спирта глицерина: Cl-CH2-C(Cl)H-CH2-Cl + NaOH→ HO-CH2-C(OH)H-CH2-OH + 3NaCl. Взаимодействие глицерина с азотной кислотой в присутствии серной кислоты приводит к образованию нитроглицерина, являющегося основой динамита: HO-CH2-C(OH)H-CH2-OH + 3HO-NO2→ O2N-CH2-C(NO2)H-CH2— NO2 +3H2O. |











