Этен
Характеристики и физические свойства этена
Этен (этилен) – бесцветный горючий газ (строение молекулы показано на рис. 1), обладающий слабым запахом. Мало растворим в воде. Хорошо растворяется в диэтиловом эфире и углеводородах.
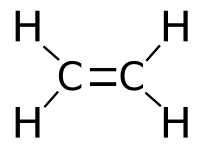
Рис. 1. Строение молекулы этилена.
Таблица 1. Физические свойства этена.
|
Молекулярная формула |
CH2=CH2 (C2H4) |
|
Молярная масса, г/моль |
28 |
|
Плотность, г/см3 |
0,001178 |
|
Температура плавления, oС |
-169,2 |
|
Температура кипения, oС |
-103,7 |
Получение этена
В промышленных объемах этен получают при переработке нефти: крекингом и дегидрированием этана. Лабораторные способы получения этилена представлены
— дегидратация этанола
CH3-CH2-OH→CH2=CH2 + H2O (H2SO4 (conc), to = 170).
— дегидрогалогенированиемоногалогенэтана
CH3-CH2-Br + NaOHalcohol→CH2=CH2 + NaBr + H2O (to).
— дегалогенирование дигалогенаэтана
Cl-CH2-CH2-Cl + Zn(Mg) →CH2=CH2 + ZnCl2(MgCl2);
— неполное гидрирование ацетилена
CH≡CH + H2→CH2=CH2 (Pd, to).
Химические свойства этена
Этен весьма реакционноспособоное соединение. Все химические превращения этилена протекают с расщеплением:
- p-связи С-С (присоединение, полимеризация и окисление)
- гидрирование
CH2=CH2 + H2→ CH3-CH3 (kat = Pt).
- галогенирование
CH2=CH2 + Br2→ BrCH-CHBr.
- гидрогалогенирование
CH2=CH2 + H-Cl → H2C-CHCl.
- гидратация
CH2=CH2 + H-OH → CH3-CH2-OH (H+, to).
- полимеризация
nCH2=CH2→ -[-CH2-CH2-]-n (kat, to).
- окисление
CH2=CH2 + 2KMnO4 + 2KOH → HO-CH2-CH2-OH + 2K2MnO4;
2CH2=CH2 + O2 → 2C2OH4 (эпоксид) (kat = Ag,to);
2CH2=CH2 + O2 → 2CH3-C(O)H (kat = PdCl2, CuCl).
- связей Сsp3-Н (в аллильном положении)
CH2=CH2 + Cl2→ CH2=CH-Cl + HCl (to=400).
- Разрыв всех связей
C2H4 + 2O2→ 2CO2 + 2H2O.
Применение этена
Основное направление использование этилена — промышленный органический синтез таких соединений как галогенопроизводные, спирты (этанол, этиленгликоль), уксусный альдегид, уксусная кислота и др. Кроме этого данное соединение в производстве полимеров.
Примеры решения задач
| Задание | В результате присоединения йода к этилену получено 98,7 г иодопроизводного. Рассчитайте массу и количество вещества этилена, взятого для реакции. |
| Решение | Запишем уравнение реакции присоединения йода к этилену:
H2C = CH2 + I2 → IH2C – CH2I. В результате реакции образовалось иодопроизводное – дийодэтан. Рассчитаем его количество вещества (молярная масса равна – 282 г/моль): n = m / M; n(C2H4I2) = m (C2H4I2) / M (C2H4I2); n(C2H4I2) = 98,7 / 282 = 0,35 моль. Согласно уравнению реакции n(C2H4I2) : n(C2H4) = 1:1, т.е. n(C2H4I2) = n(C2H4) = 0,35 моль. Тогда масса этилена будет равна (молярная масса – 28 г/моль): m = n×M; m(C2H4) = n (C2H4) ×M (C2H4); m(C2H4) = 0,35×28 = 9,8 г. |
| Ответ | Масса этилена равна 9,8 г, количество вещества этилена равно 0,35 моль. |
| Задание | Рассчитайте объем этилена, приведенный к нормальным условиям, который можно получить из технического этилового спирта C2H5OH массой 300 г. Учтите, что технический спирт содержит примеси, массовая доля которых равна 8%. |
| Решение | Запишем уравнение реакции получения этилена из этилового спирта:
C2H5OH (H2SO4) → C2H4 + H2O. Найдем массу чистого (без примесей) этилового спирта. Для этого сначала рассчитаем его массовую долю: ωpure(C2H5OH) = ωimpure(C2H5OH) – ωimpurity; ωpure(C2H5OH) = 100% — 8% = 92%. mpure(C2H5OH) =mimpure(C2H5OH) ×ωpure(C2H5OH) / 100%; mpure(C2H5OH) = 300 × 92 / 100% = 276 г. Определим количество вещества этилового спирта (молярная масса – 46 г/моль): n = m / M; n(C2H5OH) = m (C2H5OH) / M (C2H5OH); n(C2H5OH) = 276 / 46 = 3,83 моль. Согласноуравнениюреакцииn(C2H5OH) : n(C2H4) = 1:1, т.е. n(C2H5OH) = n(C2H4) = 3,83 моль. Тогда объем этилена будет равен: V = n × Vm; V(C2H4) = n(C2H4) × Vm; V(C2H4) = 3,83 × 22,4 = 85,792 л. |
| Ответ | Объем этилена равен 85,792 л. |











