Молярная масса этилового спирта
Молярная масса этилового спирта
Строение молекулы бензола показано на рис. 1. В обычных условиях представляет собой бесцветную летучую жидкость с характерным запахом и жгучим вкусом. Смешивается с водой и различными органическими растворителями, а также сам хорошо растворяет многие вещества (чаще органической природы).
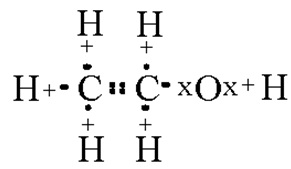
Рис. 1. Строение молекулы этилового спирта.
Брутто-формула этилового спирта – C2H5OH. Как известно, молекулярная масса молекулы равна сумме относительных атомных масс атомов, входящих в состав молекулы (значения относительных атомных масс, взятых из Периодической таблицы Д.И. Менделеева, округлим до целых чисел).
Mr(C2H5OH) = 2×Ar(С) + 6×Ar(H) + Ar(O);
Mr(C2H5OH) = 2×12 + 6×1 + 16 = 24 + 6 + 16 = 46.
Молярная масса (М) – это масса 1 моль вещества. Легко показать, что численные значения молярной массы М и относительной молекулярной массы Mrравны, однако первая величина имеет размерность [M] = г/моль, а вторая безразмерна:
M = NA × m (1 молекулы) = NA × Mr × 1 а.е.м. = (NA ×1 а.е.м.) × Mr = × Mr.
Это означает, что молярная масса этилового спирта равна 46 г/моль.
Примеры решения задач
| Задание | Вычислите, какая масса воды получится, если в реакцию с водородом вступило 16 г кислорода? |
| Решение | Запишем уравнение реакции взаимодействия водорода с кислородом:
2H2 + O2 = 2H2O. Вычислим количество вещества кислорода по формуле: n = m / M; n(O2)= m (O2)/ M(O2). Для этого необходимо указать молярную массу кислорода (значение относительной атомной массы, взятое из Периодической таблицы Д.И. Менделеева, округлим до целого числа). Как известно, молярная масса молекулы равна сумме относительных атомных масс атомов, входящих в состав молекулы (M = Mr): M(O2) = 2×Ar(O) = 2×16 = 32 г/моль. Тогда, количество вещества кислорода будет равно: n(O2)= 16 / 32 = 0,5 моль. Согласно уравнению реакции n(O2) :n(H2O) = 2 : 2, значит: n(H2O) =n(O2) = 0,5 моль. Найдем молярную массу воды (допущение, указанное при расчете молярной массы кислорода действительно и в данном случае): M(H2O) = 2×Ar(H) + Ar(O) = 2×1 + 16 = 2 +16 = 18 г/моль. Определим массу воды: m = n × M; m(H2O) = n (H2O) × M (H2O); m(H2O) = 0,5 × 16 = 8 г. |
| Ответ | Масса воды равна 8 г. |
| Задание | Вычислите, какой объём кислорода (н.у.) необходим для получения оксида серы (VI) по реакции взаимодействия с оксидом серы (IV) массой 6,4 г? |
| Решение | Запишем уравнение реакции взаимодействия кислорода с оксидом серы (IV) в результате которой образуется оксид серы (VI):
2SO2 + O2 = 2SO3. Вычислим количество вещества оксида серы (IV) по формуле: n = m / M; n(SO2)= m (SO2)/ M(SO2). Для этого необходимо указать молярную массу оксида серы (IV (значение относительной атомной массы, взятое из Периодической таблицы Д.И. Менделеева, округлим до целого числа). Как известно, молярная масса молекулы равна сумме относительных атомных масс атомов, входящих в состав молекулы (M = Mr): M(SO2) = Ar(S) + 2×Ar(O) = 32 + 2×16 = 32 + 32 = 64 г/моль. Тогда, количество вещества оксида серы (IV будет равно: n(SO2)= 6,4/ 64 = 0,1 моль. Согласно уравнению реакции n(SO2) :n(SO3) = 2 : 2, значит: n(SO3) = n(SO2) = 0,1 моль. Найдем молярную массу оксида серы (VI)(допущение, указанное при расчете молярной массы кислорода действительно и в данном случае): M(SO3) = Ar(S) + 3×Ar(O) = 32 + 3×16 = 32 + 48 = 80 г/моль. Определим массу оксида серы (VI): m = n × M; m(SO3) = n (SO3) × M (SO3); m(SO3) = 0,1 × 80 = 8 г. |
| Ответ | Масса оксида серы (VI) равна 8 г. |











