Гибридизация электронных орбиталей и геометрия молекул
В 1930 г. Слейтером и Л. Полингом была развита теория образования ковалентной связи за счет перекрывания электронных орбиталей – метод валентных связей. В основе этого метода лежит метод гибридизации, который описывает образование молекул веществ за счет «смешивания» гибридных орбиталей («смешиваются» не электроны, а орбитали).
Определение типа гибридизации молекул с ковалентной связью
Определить тип гибридизации можно только для молекул с ковалентной связью типа АВn, где n больше или равно двум, А – центральный атом, В – лиганд. В гибридизацию вступают только валентные орбитали центрального атома.
Определим тип гибридизации на примере молекулы BeH2.
Первоначально записываем электронные конфигурации центрального атома и лиганда, рисуем электронно-графические формулы.
4Be 1s22s2

1H1s1

Атом бериллия (центральный атом) имеет вакантные 2p-орбитали, поэтому, чтобы принять по одному электрону от каждого атома водорода (лиганд) для образования молекулы BeH2 ему необходимо перейти в возбужденное состояние:
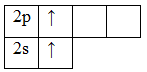
Образование молекулы BeH2 происходит за счет перекрывания валентных орбиталей атома Be
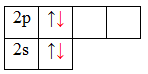
* красным цветом обозначены электроны водорода, черным – бериллия.
Тип гибридизации определяют по тому, какие орбитали перекрылись, т.о., молекула BeH2 находитс в sp – гибридизации.
Помимо молекул состава ABn, методом валентных связей можно определить тип гибридизации молекул с кратными связями. Рассмотрим на примере
молекулы этилена C2H4. В молекуле этилена кратная двойная связь, которая образована ![]() и
и ![]() –связями. Чтобы определить гибридизацию,
записываем электронные конфигурации и рисуем электронно-графические формулы атомов, входящих в состав молекулы:
–связями. Чтобы определить гибридизацию,
записываем электронные конфигурации и рисуем электронно-графические формулы атомов, входящих в состав молекулы:
6C 2s22s22p2
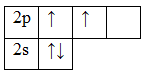
1H1s1

У атома углерода имеется еще одна вакантная p-орбиталь, следовательно, чтобы принять 4 атома водорода ему необходимо перейти в возбужденное состояние:
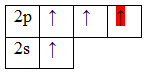
Одна p-орбиталь необходима для образования ![]() -связи (выделена красным цветом), поскольку
-связи (выделена красным цветом), поскольку ![]() -связь образуется за счет перекрывания «чистых» (негибридных) p —
орбиталей. Остальные валентные орбитали идут в гибридизацию. Таким образом этилен находится в гибридизации sp2.
-связь образуется за счет перекрывания «чистых» (негибридных) p —
орбиталей. Остальные валентные орбитали идут в гибридизацию. Таким образом этилен находится в гибридизации sp2.
Определение геометрической структуры молекул
Геометрическую структуру молекул, а также катионов и анионов состава АВn можно с помощью метода Гиллеспи. В основе этого метода – валентные пары электронов. На геометрическую структуру оказывают влияние не только электроны, участвующие в образовании химической связи, но и неподеленные электронные пары. Каждую неподеленную пару электронов в методе Гиллеспи обозначают Е, центральный атом – А, лиганд – В.
Если неподеленных электронных пар нет, то состав молекул может быть АВ2 (линейная структура молекулы), АВ3 (структура плоского треугольника), АВ4 (тетраэдрическая структура), АВ5 (структура тригональной бипирамиды) и АВ6 (октаэдрическая структура). От базисных структур могут быть получены производные, если вместо лиганда появляется неподеленная электронная пара. Например: АВ3Е (пирамидальная структура), АВ2Е2 (угловая структура молекулы).
Чтобы определить геометрическую структуру (строение ) молекулы необходимо определить состав частицы, для чего вычисляют количество неподеленных лектронных пар (НЕП):
НЕП = (общее число валентных электронов – число электронов, пошедших на образование связи с лигандами) / 2
На связь с H, Cl, Br, I, F уходит по 1-му электрону от А, на связь с O – по 2 электрона, а на связь с N – по 3 электрона от центрального атома.
Рассмотрим на примере молекулы BCl3. Центральный атом – B.
5B 1s22s22p1
НЕП = (3-3)/2 = 0, следовательно неподеленных электронных пар нет и молекула имеет структуру АВ3 – плоский треугольник.
Подробно геометрическое строение молекул разного состава представлено в табл. 1.
Таблица 1. Пространственное строение молекул
|
Формула молекулы |
Тип гибридизации |
НЕП |
Тип молекулы |
Геометрия молекулы |
Пример |
|
АВ2 |
sp |
0 |
АВ2 |
линейная |
BeH2 |
|
АВ3 |
sp2 |
0 |
АВ3 |
треугольная |
BCl3 |
|
1 |
АВ2Е |
угловая |
GeF2 |
||
|
АВ4 |
sp3 |
0 |
АВ4 |
тетраэдр |
CH4 |
|
1 |
АВ3Е |
тригональная пирамида |
NH3 |
||
|
2 |
АВ2Е2 |
угловая |
H2O |
||
|
АВ5 |
sp3d |
0 |
АВ5 |
тригональная бипирамида |
PF5 |
|
1 |
АВ4Е |
дисфеноид |
SCl4 |
||
|
2 |
АВ3Е2 |
Т-образная |
ICl3 |
||
|
3 |
АВ2Е3 |
линейная |
XeF2 |
||
|
АВ6 |
sp3d2 |
0 |
АВ6 |
октаэдр |
SF6 |
|
1 |
АВ5Е |
квадратная пирамида |
IF5 |
||
|
2 |
АВ4Е2 |
квадрат |
XeF4 |
Примеры решения задач
| Задание | Определите с помощью метода валентных связей тип гибридизации молекулы метана (CH4) и его геометрическую структуру по методу Гиллеспи |
| Решение |
6С 2s22s22p2
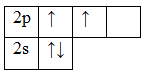
1H1s1 
Чтобы принять 4 лиганда атому углерода необходимо перейти в возбужденное состояние, следовательно электроны 2s-орбитали распарятся и один из них перейдет на p-орбиталь – в гибридизации будут участвовать все валентные орбитали атома углерода. Тип гибридизации sp3. Рассчитываем НЕП : (4 – 4)/2=0, следовательно метан имеет тетраэдрическую структуру. |
| Ответ | Тип гибридизации sp |
| Задание | Определите с помощью метода валентных связей тип гибридизации молекулы BCl3 и его геометрическую структуру по методу Гиллеспи |
| Решение |
5B 1s22s22p1
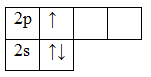
17Сl 1s22s22p63s23p5 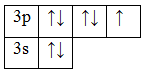
Атому бора необходимо перейти в возбужденное состояние, чтобы принять 3 атома хлора: 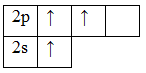
Тип гибридизации sp2. Рассчитываем НЕП : (3 – 3)/2=0, следовательно молекула BCl3 имеет структуру плоского треугольника. |
| Ответ | Тип гибридизации sp |











