Валентность хрома
Общие сведения о валентности хрома
Хром в виде простого вещества – серовато-белый блестящий металл. Имеет структуру объемно-центрированной кубической решетки.Плотность – 7,2 г/см3. Температуры плавления и кипения равны 1890oС и 2680oС, соответственно.
Валентность хрома в соединениях
Хром находится в четвертом периоде в VIB группе Периодической таблицы Д.И. Менделеева. Порядковый номер равен 24. В ядре атома хрома содержится 24 протона и 28 нейтронов (массовое число равно 52). В атоме хрома есть четыре энергетических уровня, на которых находятся 24 электрона (рис. 1).
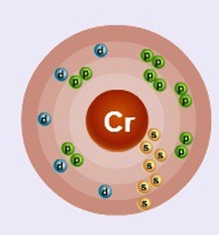
Рис. 1. Строения атома хрома.
Электронная формула атома хрома в основном состоянии имеет следующий вид:
1s22s22p63s23p63d54s1.
А энергетическая диаграмма (строится только для электронов внешнего энергетического уровня, которые по-другому называют валентными):
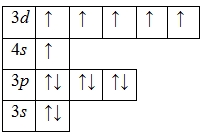
Наличие шести неспаренных электронов свидетельствует о том, что хром в своих соединениях может проявлять валентность IV (CrVIO3, CrVICl6, CrIVO2Cl6, K2CrVI2O7 и т.д.).
Известно, что для хрома также характерны валентности II (CrIIO, CrII(OH)2, CrIICl2) и III(CrIII2O3, CrIII(OH)3, KCrIIIO2, CrIIICl3).
Примеры решения задач
| Задание | Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
Cr → CrCl3 →Cr(OH)3 → Cr2(SO4)3. |
| Ответ | Хром взаимодействует с простыми веществами, например, с хлором:
2Cr+ 6Cl2 → 2CrCl3. При действии на хлорид хрома (III) щелочи можно получить гидроксид хрома (III): CrCl3 + 3NaOH → Cr(OH)3 + 3NaCl. Гидроксид хрома (III) вступает в реакцию нейтрализации с серной кислотой, в результате которой образуется сульфат хрома (III) и вода: 2Cr(OH)3+ 3H2SO4→ Cr2(SO4)3 + 6H2O. |
| Задание | Оксид хрома (VI) массой 2 г растворили в воде массой 500 г. Рассчитайте массовую долю хромовой кислоты H2CrO4 в полученном растворе. |
| Решение | Запишем уравнение реакции получения хромовой кислоты из оксида хрома (VI):
CrO3 + H2O = H2CrO4. Найдем массу раствора: msolution = m(CrO3) + m (H2O) = 2+500 = 502 г. Для того, чтобы рассчитать массу растворенного вещества хромовой кислоты, определим количество вещества оксида хрома (VI) (молярная масса – 100 г/моль): n = m / M; n (CrO3) = m (CrO3) / M (CrO3); n (CrO3) = 2 / 100 = 0,02 моль. Согласно уравнению реакции n(CrO3) :n(H2CrO4) = 1:1, значит, n(CrO3) = n(H2CrO4) = 0,02 моль. Тогда масса хромовой кислоты будет равна (молярная масса – 118 г/моль): m = n × M; m (H2CrO4) = n (H2CrO4) × M (H2CrO4); m (H2CrO4) = 0,02 × 118 = 2,36 г. Массовая доля хромовой кислоты в растворе составляет: ω = msolute / msolution × 100%; ω(H2CrO4)=msolute(H2CrO4)/ msolution × 100%; ω (H2CrO4)=2,36 / 502 × 100% = 0,47 %. |
| Ответ | Массовая доля хромовой кислоты равна 0,47%. |











