Валентность водорода
Общие сведения о валентности водорода
При температуре ниже -240oС (критическая температура водорода) он под давлением сжижается. Если испарять полученную жидкость, то образуется твердый водород в виде прозрачных кристаллов, плавящихся при -259,2oС.
Водород – самый легкий из всех газов, он в 14,5 раз легче воздуха; масса 1 л водорода при нормальных условиях равна 0,09 г. В воде водород растворим очень мало, но в некоторых металлах, например в никеле, паладии, платине, растворяется в значительных количествах.
Водород имеет три изотопа: протий 1H, дейтерий 2H или D и тритий 3H или T. Их массовые числа равны 1, 2 и 3. Протий и дейтерий стабильны, тритий – радиоактивен. Ядро атома водорода 1H содержит один протон. Ядра дейтерия и трития включают кроме одного протона соответственно один и два нейтрона.
Молекула водорода состоит из двух атомов – H2.
Валентность водорода в соединениях
В ядре атома водорода содержится один протон, а по единственной орбите вокруг него движется один электрон (рис. 1).
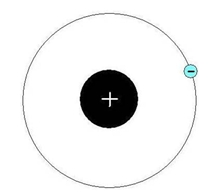
Рис. 1. Строение атома водорода.
Электронная формула атома водорода в основном состоянии будет выглядеть следующим образом:
1H 1s1.
А энергетическая диаграмма:
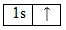
Наличие одного неспаренного электрона свидетельствует о том, что для водорода характерна валентность равная I. Этот факт также подтверждается и тем, что водород расположен в IA группе Периодической таблицы Д.И. Менделеева, а, как известно, высшая валентность химического элемента определяется номером группы, в которой он находится. Валентность водорода постоянна во всех соединениях (BaHI2, HICl, NaOHI, Ca(HICO3)2и т.д.)
Примеры решения задач
| Задание | Могут ли реагировать между собой бинарные водородные соединения? Дайте обоснованный ответ. Приведите уравнения возможных реакций на примере водородных соединений элементов второго и третьего периодов Периодической системы. |
| Ответ | Бинарные водородные соединения элементов второго и третьего периодов могут вступать во взаимодействие друг с другом, проявляя как кислотно-основные, так и окислительно-восстановительные свойства. Например, между собой реагируют:
В этих реакциях аммиак и фосфин проявляют свойства оснований, а вода, хлороводород и фтороводород – свойства кислот. Окислительно-восстановительные реакции протекают при взаимодействии гидридов лития и натрия с водой, хлороводородом и сероводородом: В этих реакциях гидриды металлов выступают в роли восстановителей, а вода, хлороводород и сероводород – в роли окислителей. |
| Задание | Некоторый элемент образует гидрид ЭН3, массовая доля водорода в котором равна 8,82%. Определите этот элемент. |
| Решение | Рассчитаем относительную молекулярную массу ЭН3, воспользовавшись расчетной формулой массовой доли химического элемента в веществе:
ω (Э) = Ar (Э) × n / Mr× 100%; Mr (ЭН3) = Ar (Н) × 3 / ω (Н) × 100%; Mr (ЭН3) = 1 × 3 / 8,82× 100% = 34. Рассчитаем относительную атомную массу элемента: Ar (Э) + 1 × 3 = 34; Ar (Э) = 31. Следовательно, искомый элемент – фосфор. |
| Ответ | Этот элемент — фосфор. |











