Молярная масса водорода
Молярная масса водорода
M = m / n.
Молярную массу обычно выражают в г/моль, реже в кг/кмоль. Поскольку в одном моле любого вещества содержится одинаковое число структурных единиц, то молярная масса вещества пропорциональная массе соответствующей структурной единицы, т.е. относительной атомной массе данного вещества (Mr):
M = κ × Mr,
где κ – коэффициент пропорциональности, одинаковый для всех веществ. Относительная молекулярная масса – величина безразмерная. Её вычисляют, используя относительные атомные массы химических элементов, указанных в Периодической системе Д.И. Менделеева.
Относительная атомная масса атомарного водорода равна 1,008 а.е.м. Его относительная молекулярная масса будет равна 1,008, а молярная масса:
M(H) = Mr (H) × 1 моль = 1,008 г/моль.
Известно, что молекула водорода двухатомна – H2, тогда, относительная атомная масса молекулы водорода будет равна:
Ar(H2) = 1,008 × 2 = 2,016 а.е.м.
Относительная молекулярная масса молекулы водорода будет равна 2,016, а молярная масса:
M(H) = Mr (H) × 1 моль = 2,016 г/моль или просто 2 г/моль.
Водород представляет собой газ без цвета и запаха (схема строения атома представлена на рис. 1), который при температуре (-240oC) и под давлением способен сжижаться, а при быстром испарении полученной жидкости переходить в твердое состояние (прозрачные кристаллы).
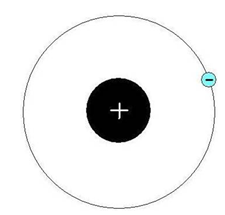
Рис. 1. Строение атома водорода.
Молекулярную массу вещества в газообразном состоянии можно определить, используя понятие о его молярном объеме. Для этого находят объем, занимаемый при нормальных условиях определенной массой данного вещества, а затем вычисляют массу 22,4 л этого вещества при тех же условиях.
Для достижения данной цели (вычисление молярной массы) возможно использование уравнения состояния идеального газа (уравнение Менделеева-Клапейрона):
pV = mRT / M,
где p – давление газа (Па), V – объем газа (м3), m – масса вещества (г), M – молярная масса вещества (г/моль), Т – абсолютная температура (К), R – универсальная газовая постоянная равная 8,314 Дж/(моль×К).
Примеры решения задач
| Задание | Могут ли реагировать между собой бинарные водородные соединения? Дайте обоснованный ответ. Приведите уравнения возможных реакций на примере водородных соединений элементов второго и третьего периодов Периодической системы. |
| Ответ | Бинарные водородные соединения элементов второго и третьего периодов могут вступать во взаимодействие друг с другом, проявляя как кислотно-основные, так и окислительно-восстановительные свойства. Например, между собой реагируют:
В этих реакциях аммиак и фосфин проявляют свойства оснований, а вода, хлороводород и фтороводород – свойства кислот. Окислительно-восстановительные реакции протекают при взаимодействии гидридов лития и натрия с водой, хлороводородом и сероводородом: В этих реакциях гидриды металлов выступают в роли восстановителей, а вода, хлороводород и сероводород – в роли окислителей. |
| Задание | Некоторый элемент образует гидрид ЭН3, массовая доля водорода в котором равна 8,82%. Определите этот элемент. |
| Решение | Рассчитаем относительную молекулярную массу ЭН3, воспользовавшись расчетной формулой массовой доли химического элемента в веществе:
ω (Э) = Ar (Э) × n / Mr × 100%; Mr (ЭН3) = Ar (Н) × 3 / ω (Н) × 100%; Mr (ЭН3) = 1 × 3 / 8,82 × 100% = 34. Рассчитаем относительную атомную массу элемента: Ar (Э) + 1 × 3 = 34; Ar (Э) = 31. Следовательно, искомый элемент – фосфор. |
| Ответ | Фосфор |











