Валентность фтора
Общие сведения о валентности фтора
Фтор самый электроотрицательный элемент. В обычных условиях фтор представляет собой газ бледно-желтого цвета. Ядовит. В малых концентрациях запах фтора напоминает запах озона и хлора одновременно.
Молекула фтора двухатомна F2. Обладает самой низкой поляризуемостью среди галогенов. Температура плавления фтора аномально низкая. Не растворим в воде, т.к. разлагает ее (2F2 + 2H2O = 4HF + O2).
Валентность фтора в соединениях
Фтор — девятый по счету элемент Периодической таблицы Д.И. Менделеева. Он находится во втором периоде во VIIA группе. В ядре атома фтора содержится 9 протонов и 10 нейтронов (массовое число равно 19). В атоме фтора есть два энергетических уровня, на которых находятся 9 электронов (рис. 1).
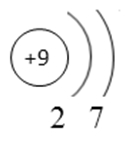
Рис. 1. Строения атома фтора.
Электронная формула атома фтора в основном состоянии имеет следующий вид:
1s22s22p5.
А энергетическая диаграмма (строится только для электронов внешнего энергетического уровня, которые по-другому называют валентными):
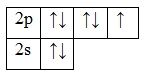
Наличие одного неспаренных электрона свидетельствует о том, что фтор проявляет валентность I во всех своих соединения (HFI, KFIи т.д.). Валентность постоянная. Фтор – один из элементов, для которого не характерна высшая валентность, определяемая по номеру группы.
Примеры решения задач
| Задание | Валентность элемента равна: 1) числу образуемых им σ-связей; 2) числу образуемых им π-связей; 3) числу образуемых им ковалентных связей; 4) степени окисления с противоположным знаком. |
| Ответ | Под валентностью понимают свойство атома химического элемента присоединять или замещать определенное число атомов другого элемента, т.е., валентность — это количество ковалентных химических связей, которые атом данного химического элемента может образовывать с другими атомами. |
| Задание | Число неспаренных электронов в атоме бора в основном состоянии такое же, как и в атоме: 1) рубидия; 2) кремния; 3) кислорода; 4) кальция. |
| Решение | Число неспаренных электронов в атоме химического элемента чаще всего равно одному из значений валентности, которые проявляет этот элемент. Чтобы определить число неспаренных электронов в атоме бора в основном состоянии запишем электронную формулу этого элемента:
5B 1s22s22p1. На внешнем электронном уровне бора находится 3 электрона из которых только один неспаренный. Один неспаренный электрон в основном состоянии также имеет рубидий, поскольку он расположен в IA группе и на его внешнем электронном уровне находится всего один электрон, который, естественно, является неспаренным. |
| Ответ | Вариант 1. |











