Этан
Характеристики и физические свойства этана
Не имеет вкуса. Не растворим в воде. Проявляет слабое наркотическое действие.
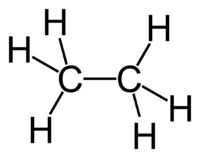
Рис. 1. Строение молекулы этана.
Таблица 1. Физические свойства этан.
|
Молекулярная формула |
C2H6 |
|
Молярная масса |
30 |
|
Плотность (20oС), кг/м3 |
1,0621 |
|
Температура плавления, oС |
-182,8 |
|
Температура кипения, oС |
-88,6 |
Получение этана
В больших объемах этан получают из попутного нефтяного газа и газов нефтекрекинга.
В лабораторных условиях этан получают следующими способами:
— гидрированием непредельных углеводородов
CH2=CH2 + H2→CH3-CH3 (kat = Ni, to);
— восстановлением галогеналканов
C2H5I + HI →C2H6 + I2 (to);
— по реакции щелочного плавления солей одноосновных органических кислот
C2H5-COONa + NaOH → C2H6 + Na2CO3 (to);
— взаимодействием галогеналканов с металлическим натрием (реакция Вюрца)
2CH3Br + 2Na → CH3-CH3 + 2NaBr.
Химические свойства этана
В обычных условиях этан не реагирует с концентрированными кислотами, расплавленными и концентрированными щелочами, щелочными металлами, галогенами (кроме фтора), перманганатом калия и дихроматом калия в кислой среде.
Для этана наиболее характерны реакции, протекающие по радикальному механизму. Энергетически более выгоден гомолитический разрыв связей C-H и C-C, чем их гетеролитический разрыв.
Все химические превращения этана протекают с расщеплением:
- cвязей C-H
- галогенирование (SR)
CH3-CH3 + Br2→ CH3-CH2Br + HBr (hv).
- нитрование (SR)
CH3-CH3 + HONO2 (dilute)→ CH3-C(NO2)H2+ H2O (to).
- сульфохлорирование (SR)
C2H6 + SO2 + Cl2→ C2H5-SO2Cl + HCl↑ (hv).
- дегидрирование
CH3-CH3→ CH2=CH2+ H2 (kat = Ni, to).
- связей C-H и C-C
- окисление
2C2H6 + 7O2→4CO2 + 6H2O (to).
Применение этана
Этан используется как сырье в химической промышленности в основном для получения этилена.
Примеры решения задач
| Задание | Определите массу хлора, необходимого для хлорирования по первой стадии 4,5 л этана. |
| Решение | Запишем уравнение реакции хлорирования этана:
C2H6 + Cl2 = C2H5Cl + HCl. Найдем количество вещества этана: n = V/ Vm; n(C2H6) = V(C2H6) / Vm; n(C2H6) = 4,5 / 22,4 = 0,2 моль. Согласно уравнению реакции n(C2H6) : n(Cl2) = 1:1, значит,количество моль хлора равно: n(Cl2) = n(C2H6) =0,2моль. Тогда, масса хлора будет равна (молярная масса – 71 г/моль): m(Cl2) = n(Cl2) × M(Cl2); m(Cl2) = n(Cl2) × M(Cl2); m(Cl2)=0,2 ×71= 14 г. |
| Ответ | Масса хлора равна 14 г. |
| Задание | Рассчитайте объемы хлора и этана, приведенные к нормальным условиям, которые потребуются для получения дихлорэтана массой 10,5 г. |
| Решение | Запишем уравнение реакции хлорирования этана до дихлорэтана (реакция происходит под действием УФ-излучения):
C2H6 + 2Cl2 = C2H4Cl2+ 2HCl. Рассчитаем количество вещества дихлорэтана (молярная масса равна – 99 г/моль): n = m / M; n(C2H4Cl2) = m (C2H4Cl2) / M (C2H4Cl2); n(C2H4Cl2) = 10,5 / 99 = 0,12 моль. Согласно уравнению реакции n(C2H4Cl2) : n(C2H6) = 1:1, т.е. n(C2H4Cl2) = n(C2H6) = 0,12 моль. Тогда объем этана будет равен: V = n × Vm; V(C2H6) = n(C2H6) × Vm; V(C2H6) = 0,12 × 22,4 = 2,7 л. По уравнению реакции найдем количество вещества хлора. n(C2H4Cl2) : n(Cl2) = 1:2, т.е. n(Cl2) = 2 × n(C2H4Cl2) = 2 × 0,12 = 0,24 моль. Тогда объем хлора будет равен: V = n × Vm; V(Cl2) = n(Cl2) × Vm; V(Cl2) = 0,24 × 22,4 = 5,4л. |
| Ответ | Объемы хлора и этана равны 5,4 и 2,7 л соответственно. |











