Строение атома магния
Общие сведения о строении атома магния
Порядковый номер равен 12. Заряд ядра равен +12. Атомный вес – 24,132 а.е.м.
Электронное строение атома магния
Магний расположен в третьем периоде, значит, он имеет три оболочки, одна из которых внешняя, содержащая валентные электроны. Атом магния имеет положительно заряженное ядро (+12), в котором имеется 12 протонов и 12 нейтронов (разница между атомным весом и порядковым номером). По орбитам вокруг ядра движутся 12 электронов.
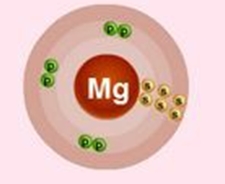
Рис. 1. Схематичное изображение строения атома магния.
Электронную конфигурацию атома магния можно записать двояко:
+12Mg)2)8)2;
1s22s22p63s2.
Магний относится к семейству s-элементов. Энергетическая диаграмма атома магния (на ней изображаются только валентные электроны) имеет вид:

В результате химического взаимодействия магний теряет свои валентные электроны, т.е. является их донором, и превращается в положительно заряженный ион (Mg2+):
Mg0 –2e → Mg2+;
В соединениях магний проявляет степень окисления +2.
Примеры решения задач
| Задание | Химическому элементу главной подгруппы соответствует высший оксид состава RO3. Какова электронная конфигурация внешнего энергетического уровня атома этого элемента? |
| Ответ | Необходимо определить к какой группе Периодической системы относится элемент, образующий высший оксид состава RO3. Поскольку в оксидах кислород проявляет постоянную валентность равную II, то высшая валентность элемента в оксиде RVIOII3 равна VI.
Отсюда следует, что это элемент VIA группы, в его атоме 6 валентных электронов. Этому требованию соответствует элемент с электронной формулой ns2np4. |
| Задание | Исходя из строения внешнего уровня атома меди, объясните, какие значения степени окисления могут быть характерны для меди. |
| Решение | Напишем электронную формулу атома меди в основном состоянии, учитывая, что для меди характерен проскок электрона с 4s –подуровня на 3d-подуровень, который объясняется тем, что завершенный подуровень энергетически более выгоден:
1s22s22p63s23p63d104s1. 4s-электрон является валентным. В возбужденном состоянии один из d-электронов возвращается на 4-й уровень, таким образом там оказывается 2 валентных электрона. Итак, для меди характерны два значения степени окисления: +1 и +2. |
| Ответ | +1 и +2 |











