Строение атома лития
Общие сведения о строении атома лития
Порядковый номер равен 3. Заряд ядра равен +3. Атомный вес – 6,941а.е.м.
Электронное строение атома лития
Поскольку литий расположен во втором периоде, он имеет две оболочки, одна из которых носит название внешней. Электроны, расположенные на внешней оболочке, называются валентными и участвуют в образовании химических связей. Атом лития имеет положительно заряженное ядро (+3), в котором имеется 3 протона и 4 нейтрона (разница между атомным весом и порядковым номером). По орбитам вокруг ядра движутся 3 электрона.
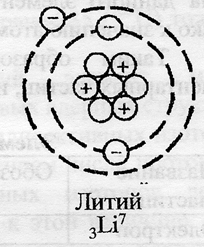
Рис. 1. Схематичное изображение строения атома лития.
Электронную конфигурацию атома лития можно записать двояко:
+3 Li)2)1;
1s22s1.
Литий, так же, как и водород и гелий относится к семейству s-элементов. Энергетическая диаграмма атома лития (на ней изображаются только валентные электроны) имеет вид:
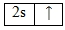
В результате химического взаимодействия литий теряет свой валентный электрон, т.е. является его донором, и превращается в положительно заряженный ион (Li+):
Li0 –e → Li+;
В соединениях литий проявляет степень окисления +1.
Примеры решения задач
| Задание | Запишите электронные конфигурации атомов элементов с атомными номерами 7, 16, 21. |
| Ответ | Химический элемент с атомным номером 7 – это азот. Он находится во втором периоде, следовательно, имеет две орбитали. Расположение азота в V группе Периодической таблицы свидетельствует о наличии на внешнем энергетическом уровне 5-ти валентных электронов:
+7 N)2)5; 1s22s22p3. Химический элемент с атомным номером 16 – это сера. Она находится в третьем периоде, следовательно, имеет три орбитали. Расположение серы в VI группе Периодической таблицы свидетельствует о наличии на внешнем энергетическом уровне 6-ти валентных электронов: +16 S)2)8)6; 1s22s22p63s23p4. Химический элемент с атомным номером 21 – это скандий. Он находится в четвертом периоде, следовательно, имеет четыре орбитали. Расположение скандия в III группе Периодической таблицы свидетельствует о наличии на внешнем энергетическом уровне 3-х валентных электронов: +21 Sc)2)8)8)3; 1s22s22p63s23p63d24s2. |
| Задание | Укажите номер периода и номер группы (главная или побочная подгруппа) для элементов с электронными конфигурациями атомов:
а) 1s22s22p63s23p63d54s2; б) ls22s22p63s23p63d104s24p5; в) ls22s22р63s23р63d104s24р64d105s1; г) [Rn]7s2. |
| Ответ | Чтобы определить порядковый номер химического элемента по его электронной конфигурации, записанной в виде а)-в), нужно сложить все электроны. Если же конфигурация записана, как в случае г), надо прибавить к порядковому номеру элемента, указанного в квадратных скобках число электронов, «привязанных» к орбиталям.
а) 15 – это фосфор. Расположен в третьем периоде VA (главная подгруппа) группе; б) 35 – это бром. Расположен в четвертом периоде VIIA(главная подгруппа) группе; в) 47 – это серебро. Элемент расположен в пятом периоде IB (побочная подгруппа) группе; г) 88 – это радий. Расположен в седьмом периоде IIA(главная подгруппа) группе. |











