Строение атома гелия
Общие сведения о строении атома гелия
Порядковый номер равен 2. Заряд ядра равен +2. Атомный вес – 4,003 а.е.м.
Электронное строение атома гелия
Атом гелия состоит из положительно заряженного ядра (+2), вокруг которого по атомным оболочкам (орбиталям) движутся два электрона. Поскольку гелий расположен в первом периоде, оболочка всего одна. Схема строения атома гелия представлена на рисунке 1:
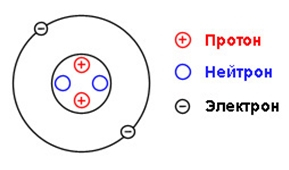
Рис. 1. Схема строения атома гелия.
Электронную конфигурацию атома гелия можно записать двояко:
+2 He)2;
1s2.
Гелий, так же, как и водород относится к семейству s-элементов. Энергетическая диаграмма атома гелия имеет вид:
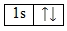
Энергетический уровень атома гелия завершенный, поскольку на s-орбитали может располагаться всего два электрона. Именно поэтому гелий относят к инертным газам. Химически он малоактивен.
Примеры решения задач
| Задание | Расположите энергетические подуровни в последовательности их заполнения электронами:
а) 3р, 3d, 4s, 4р; б) 4d, 5s, 5р, 6s; в) 4f, 5s, 6р; 4d, 6s; г) 5d, 6s, 6р, 7s, 4f. |
| Решение | Энергетические подуровни заполняются электронами в соответствии с правилами Клечковского. Обязательным условием является минимальное значение суммы главного и орбитального квантового чисел. Для s-подуровня характерно число 0, p – 1, d – 2 и f-3.Второе условие – первым заполняется подуровень с наименьшим значением главного квантового числа. |
| Ответ | а) Орбиталям 3р, 3d, 4s, 4р будут соответствовать числа 4, 5, 4 и 5. Следовательно заполнение электронами будет происходить в следующей последовательности: 3p, 4s, 3d, 4p.
б) Орбиталям 4d, 5s, 5р, 6s будут соответствовать числа 7, 5, 6 и 6. Следовательно заполнение электронами будет происходить в следующей последовательности: 5s, 5p, 6s, 4d. в) Орбиталям 4f, 5s, 6р; 4d, 6s будут соответствовать числа 7, 5, 76 и 6. Следовательно заполнение электронами будет происходить в следующей последовательности: 5s, 4d,6s, 4f, 6р. г) Орбиталям 5d, 6s, 6р, 7s, 4f будут соответствовать числа 7, 6, 7, 7 и 7. Следовательно заполнение электронами будет происходить в следующей последовательности: 6s, 4f, 5d, 6р, 7s. |
| Задание | Укажите количество электронных слоев в атомах элементовс атомными номерами 2, 8, 19, 33, 40, 79. |
| Ответ | Элемент с атомным номером 2 – это гелий, он расположен в первом периоде, следовательно, имеет всего один электронный слой.
Элемент с атомным номером 8 – это кислород, он расположен во втором периоде, следовательно, имеет два электронных слоя. Элемент с атомным номером 19 – это калий, он расположен в четвертом периоде, следовательно, имеет четыре электронных слоя. Элемент с атомным номером 33 – это мышьяк, он расположен в четвертом периоде, следовательно, имеет четыре электронных слоя. Элемент с атомным номером 40 – это цирконий, он расположен в пятом периоде, следовательно, имеет пять электронных слоев. Элемент с атомным номером 79 – это золото, он расположен в шестом периоде, следовательно, имеет шесть электронных слоев. |











