Формула янтарной кислоты
Определение и формула янтарной кислоты
В обычных условиях представляет собой бесцветные кристаллы, хорошо растворимые в воде и этаноле и нерастворимые в бензоле, бензине, хлороформе. Температура плавления 183oC, при нагревании до температуры 235oC переходит в янтарный ангидрид.
Химическая формула янтарной кислоты
Химическая формула янтарной кислоты может быть записана двояко: HOOC-CH2-CH2-COOH или С4H6O4. Она показывает качественный и количественный состав молекулы (сколько и каких атомов входит в конкретное соединение) По химической формуле можно вычислить молекулярную массу салициловой кислоты (Ar(С) = 12 а.е.м., Ar(Н) = 1 а.е.м., Ar(О) = 16 а.е.м.):
Mr(HOOC-CH2-CH2-COOH) = 4×Ar(С) + 6×Ar(Н) + 4×Ar(О);
Mr(HOOC-CH2-CH2-COOH) = 4×12 + 6×1 + 4×16 = 48 + 6 + 64 = 118.
Графическая (структурная) формула янтарной кислоты
Структурная (графическая) формула является более наглядной, она отражает то, как атомы связаны между собой внутри молекулы янтарной кислоты (рис. 1).
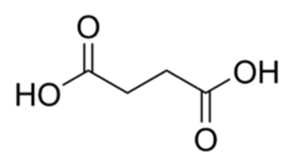
Рис. 1. Графическая формула янтарной кислоты
Примеры решения задач
| Задание | Соединение фосфора с бромом имеет массу 81,3 г, содержание фосфора в нем составляет 9,3 г. Определите простейшую формулу вещества. |
| Решение | Для того, чтобы узнать, в каких отношениях находятся химические элементы в составе молекулы необходимо найти их количество вещества. Известно, что для нахождения количества вещества следует использовать формулу:
n = m / M. Вычислим массу брома в соединении: m (Br) =81,3 — m(P) = 81,3–9,3 = 72 г. Найдем молярные массы брома и фосфора (значения относительных атомных масс, взятых из Периодической таблицы Д.И. Менделеева, округлим до целых чисел). Известно, что M = Mr, значит M(Br)= 80 г/моль, Ar(P)= 31 г/моль. Тогда, количество вещества этих элементов равно: n (Br) = m (Br) / M (Br); n (Br) = 72 / 80 = 0,9 моль. n (P) = m (P) / M (P); n (P) = 9,3 / 31 = 0,3 моль. Найдем мольное отношение: n(P) :n(Br) = 0,3 : 0,9 = 1 : 3, т.е. формула соединения фосфора и брома имеет вид PBr3. |
| Ответ | PBr3 |
| Задание | Найдите простейшую формулу соединения, имеющего следующий состав в массовых долях (%): натрия – 42, фосфора – 19, кислорода – 39. |
| Решение | Массовая доля элемента Х в молекуле состава НХ рассчитывается по следующей формуле:
ω (Х) = n × Ar (X) / M (HX) × 100%. Обозначим количество моль элементов, входящих в состав соединения за «х» (натрий), «у» (фосфор) и «z» (кислород). Тогда, мольное отношение будет выглядеть следующим образом (значения относительных атомных масс, взятых из Периодической таблицы Д.И. Менделеева, округлим до целых чисел): x:y:z = ω(Na)/Ar(Na) : ω(P)/Ar(P) : ω(O)/Ar(O); x:y:z= 42/23 : 19/31 : 39/16; x:y:z= 1,83 :0,61: 2,44 = 3 : 1 : 4. Значит простейшая формула соединения натрия, фосфора и кислорода будет иметь вид Na3PO4. |
| Ответ | Na3PO4 |











