Формула яблочной кислоты
Определение и формула яблочной кислоты
В обычных условиях представляет собой бесцветные весьма гигроскопичные кристаллы (рис. 1), хорошо растворимые в воде и этаноле.

Рис. 1. Яблочная кислота. Внешний вид.
Химическая формула яблочной кислоты
Химическая формула яблочной кислоты может записываться двояко: HOOC-CH(OH)-CH2-COOH или C4H6O5. Она показывает, что в состав данной молекулы входят четыре атома углерода (Ar = 12 а.е.м.), шесть атомов водорода (Ar= 1 а.е.м.) и пять атомов кислорода (Ar = 16 а.е.м.). По химической формуле можно вычислить молекулярную массу яблочной кислоты:
Mr(HOOC-CH(OH)-CH2-COOH) = 4×Ar(C) + 6×Ar(H) + 5×Ar(O);
Mr(HOOC-CH(OH)-CH2-COOH) = 4×12 + 6×1 + 5×16 = 48 + 6 + 80 = 134.
Структурная (графическая) формула яблочной кислоты
Структурная (графическая) формула яблочной кислоты является более наглядной. Она показывает то, как связаны атомы между собой внутри молекулы (рис. 2).
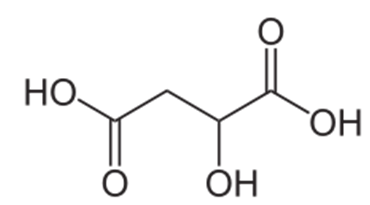
Рис. 2. Яблочная кислота. Графическая формула.
Примеры решения задач
| Задание | Найдите химическую формулу вещества, в состав которого входит 10 массовых частей кальция, 7 массовых частей азота и 24 массовых части кислорода. |
| Решение | Для того, чтобы узнать, в каких отношениях находятся химические элементы в составе молекулы необходимо найти их количество вещества. Известно, что для нахождения количества вещества следует использовать формулу:
n = m / M. Найдем молярные массы кальция азота и кислорода (значения относительных атомных масс, взятых из Периодической таблицы Д.И. Менделеева, округлим до целых чисел). Известно, что M = Mr, значит M(Ca)= 40 г/моль, М(N) = 14 г/моль, а М(О) = 16 г/моль. Тогда, количество вещества этих элементов равно: n (Ca) = m (Ca) / M (Ca); n (Ca) = 10 / 40 = 0,25 моль. n (N) = m (N) / M (N); n (N) = 7 / 14 = 0,5 моль. n (O) = m (O) / M (O); n (O) = 24 / 16 = 1,5 моль. Найдем мольное отношение: n(Ca) :n(N): n (O) = 0,25 : 0,5 : 1,5= 1 : 2 : 6, т.е. формула соединения кальция азота и кислорода имеет вид CaN2O6 или Ca(NO3)2.Это нитрат кальция. |
| Ответ | Ca(NO3)2 |
| Задание | В фосфиде кальция массой 3,62 г содержится 2,4 г кальция.Определите формулу этого соединения. |
| Решение | Для того, чтобы узнать, в каких отношениях находятся химические элементы в составе молекулы необходимо найти их количество вещества. Известно, что для нахождения количества вещества следует использовать формулу:
n = m / M. Найдем молярные массы кальция и фосфора (значения относительных атомных масс, взятых из Периодической таблицы Д.И. Менделеева, округлим до целых чисел). Известно, что M = Mr, значит M(Ca)= 40 г/моль, а М(P) = 31 г/моль. Определим массу фосфора в составе фосфида кальция: m(P) = m (CaxPy) – m(Ca); m(P) = 3,62 – 2,4 = 1,22 г. Тогда, количество вещества этих элементов равно: n (Ca) = m (Ca) / M (Ca); n (Ca) = 2,4 / 40 = 0,06 моль. n (P) = m (P) / M (P); n (P) = 1,22 / 31 = 0,04 моль. Найдем мольное отношение: n(Ca) :n(P)= 0,06 : 0,04 = 1,5 : 1 = 3 : 2, т.е. формула фосфида кальция имеет вид Ca3P2. |
| Ответ | Ca3P2 |











