Степень окисления в NH4NO3
Общие сведения о нитрате аммония и степени окисления в NH4NO3
Температура плавления – 169,6oC. Брутто-формула – NH4NO3. Молярная масса нитрата аммония равна 80,03 г/моль.
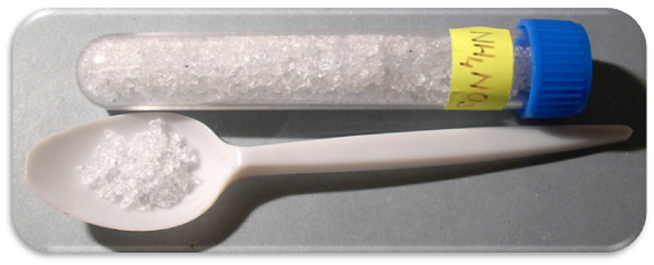
Рис. 1. Нитрат аммония. Внешний вид.
Хорошо растворим в воде (гидролизуется по катиону). Кристаллогидратов не образует. Разлагается концентрированными щелочами. В ОВР может проявлять свойства слабого окислителя и восстановителя.
NH4NO3, степени окисления элементов в нем
Чтобы определить степени окисления элементов, входящих в состав нитрата аммония, сначала необходимо разобраться с тем, для каких элементов эта величина точно известна.
Известно, что суммарная степень окисления кислотного остатка определяется числом атомов водорода, входящих в состав кислоты и записывается со знаком минус. Нитраты – это соли азотной кислоты, брутто-формула, которой имеет вид HNO3. В составе азотной кислоты имеется один атом водорода, следовательно, степень окисления кислотного остатка (нитрат-иона) равна (-1): NO31-.
Степень окисления кислорода в составе неорганических кислот, а, значит и их кислотных остатков, всегда равна (-2). Для нахождения степени окисления азота в нитрат-ионе примем её значение за «х» и определим его при помощи уравнения электронейтральности:
x + 3×(-2) = -1;
x — 6 = -1;
x = +5.
Значит степень окисления азота в составе нитрат-иона равна (+5).
Катион NH4+ является производным аммиака (гидрид водорода), степень окисления водорода, в составе которого равна (+1). Определим степень окисления азота из иона аммония аналогичным образом:
y + 4×(+1) + (+5) + 3×(-2) = 0;
y + 4 + 5 – 6 = 0;
y + 3 = 0;
y = -3.
Следовательно, степень окисления азота равна (-3):
N-3H+14N+5O-23.
Примеры решения задач
| Задание | Установите соответствие между схемой реакции и степенью окисления восстановителя:
|
||||||||||||
| Ответ | Соединение, которое является восстановителем в ОВР повышает свою степень окисления посредством передачи электронов соединению окислителю. Для того, чтобы дать правильный ответ на поставленный вопрос будем поочередно определять ОВ пары и выбирать восстановитель.
В первой реакции степень окисления изменяют элементы хлор и марганец: Cl-1 → Cl0; Mn+4 → Mn+2. Хлор повысил свою степень окисления, следовательно, хлороводород является восстановителем в этой реакции (HCl), а степень его окисления изменяется с (-1)до 0. Во второй реакции степень окисления изменяют элементы алюминий и марганец: Al0 → Al+3; Mn+2 → Mn0. Алюминий повысил свою степень окисления, следовательно, он является восстановителем в этой реакции (Al), а степень его окисления изменяется с 0 до (+3). В третьей реакции степень окисления изменяют элементы марганец и кислород: Mn+4 → Mn+2; O-2 → O0. Кислород повысил свою степень окисления, следовательно, оксид марганца (IV) является восстановителем в этой реакции (MnO2), а степень его окисления изменяется с (-2)до 0. В четвертой реакции степень окисления изменяют элементы марганец и кислород: Mn+4 → Mn+2; O-1 → O0. Кислород повысил свою степень окисления, следовательно, пероксид водорода является восстановителем в этой реакции (H2O2), а степень его окисления изменяется с (-1)до 0. |
| Задание | Наиболее низкую степень окисления хром проявляет в соединении:
а) K2Cr2O7; б) Na[Cr(H2O)2F4]; в) Cr2O3; г) Cr(OH)2. |
| Решение | Будем поочередно определять степень окисления хрома в предложенных соединениях используя для этой цели уравнение электронейтральности.
а) Степень окисления калия всегда равна (+1). Степень окисления кислорода в дихромате калия равна (-2). Примем за «х» значение степени окисления хрома: 2×1 + 2×х + 7×(-2) = 0; 2х – 12 = 0; 2х = 12; x = +6. б) Степень окисления натрия всегда равна (+1). Степень окисления фтора всегда равна (-1). Степени окисления водорода и кислорода в данном соединении равны (+1) и (-2) соответственно. Примем за «у» значение степени окисления хрома: 1 + у + 4×1 + 2×(-2) + 4×(-1)= 0; y – 3 = 0; y = +3. в) Степень окисления кислорода в оксидах равна (-2). Примем за «z» значение степени окисления хрома: 2×z + 3×(-2) = 0; 2z – 6 = 0; 2z = 6; z = +3. г) Степени окисления водорода и кислорода в данном соединении равны (+1) и (-2) соответственно. Примем за «а» значение степени окисления хрома: а + 2×(-2) + 2×1 = 0; а – 2 = 0; а = +2. Наименьшее значение степени окисления равное (+2) хром проявляет в составе соединения Cr(OH)2. |
| Ответ | Вариант (г) |











