Плотность метанола
Плотность метанола и другие его физические свойства
Он растворим в воде и некоторых полярных органических растворителях. Метиловый спирт очень ядовит. В человеческом организме он окисляется до муравьиного альдегида или муравьиной кислоты.
Основные константы метанола приведены в таблице ниже.
Таблица 1. Физические свойства и плотность метанола.
|
Плотность, г/см3 |
0,7918 |
|
Температура плавления, oС |
-97 |
|
Температура кипения, oС |
64,7 |
|
Динамическая вязкость, Па×с |
5,9×10-4 |
|
Молярная масса, г/моль |
32,04 |
Смесь воздуха с метанолом, содержание которого находится в пределах 6,98 – 35,5% взрывоопасна при температуре выше 8oС.
Химический состав и строение молекулы метанола
Химический состав молекулы метанола можно отразить при помощи эмпирической (CH3OH) и рациональной (CH3-OH) формул (рис. 1).
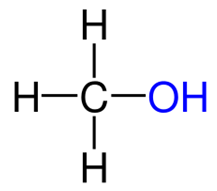
Рис. 1. Строение молекулы метилового спирта
Атом кислорода в молекуле метанола обладает большой электроотрицательностью и оттягивает на себя электронную плотность σ-связей связанных с ним атомов, в частности атома водорода. Связь O-H в молекуле метилового спирта сильно поляризована CH3-CH2→O←H. Электронная плотность в атоме водорода оказывается пониженной. Поэтому он может взаимодействовать с неподеленной парой электронов атома кислорода другой молекулы метанола. Между двумя молекулами возникает нековалентная водородная связь. Связанные между собой водородными связями молекулы метилового спирта образуют ассоциаты.
Краткое описание химических свойств и плотность метанола
Метанол является первым представителем гомологического ряда одноатомных спиртов.
За счет присутствия в воздухе кислорода, который способен выступать в роли окислителя, метиловый спирт сгорает на воздухе (светло-голубое пламя) с образованием углекислого газа и воды:
CH3OH + 2O2 = CO2 + 2H2O.
За счет наличия в молекуле метанола кислотного центра он взаимодействует со щелочными, а также некоторыми щелочноземельными металлами и их гидридами с образованием солеподобных соединений – алкоголятов:
2CH3OH + 2K = 2CH3OK + H2;
CH3OH + NaH = CH3ONa + H2.
Метиловый спирт вступает в реакции нуклеофильного замещения с галогенводородными кислотами:
CH3OH + HCl = CH3Cl + H2O.
При взаимодействии метанола с альдегидами образуются ацетали, с карбоновыми кислотами – сложные эфиры:
CH3OH + R-COH = R-CH(OH)-O-CH3;
CH3OH + R-COOH = R-COOCH3 + H2O.
В присутствии водоотнимающих реагентов и при нагревании до температуры выше 120oС метиловый спирт подвергается дегидратации:
2CH3OH = CH3-O- CH3 + H2O (H2SO4 (conc), 120oC).
Примеры решения задач
| Задание | Относительная плотность газа по водороду – 27. Массовая доля элемента водорода в нем – 18,5%, а элемента бора – 81,5%. Определите формулу газа. |
| Решение | Массовая доля элемента Х в молекуле состава НХ рассчитывается по следующей формуле:
ω (Х) = n × Ar (X) / M (HX) × 100%. Обозначим число атомов водорода в молекуле через «х», число атомов бора через «у». Найдем соответствующие относительные атомные массы элементов водорода и бора (значения относительных атомных масс, взятые из Периодической таблицы Д.И. Менделеева, округлим до целых чисел). Ar(B) = 11; Ar(H) = 1. Процентное содержание элементов разделим на соответствующие относительные атомные массы. Таким образом мы найдем соотношения между числом атомов в молекуле соединения: x:y = ω(H)/Ar(H) : ω (B)/Ar(B); x:y = 18,5/1 : 81,5/11; x:y = 18,5 : 7,41 = 2,5 : 1 = 5 : 2. Значит простейшая формула соединения водорода и бора имеет вид H5B2. Значение молярной массы газа можно определить при помощи его плотности по водороду: Mgas = M(H2) × DH2(gas); Mgas = 2 × 27 = 54 г/моль. Чтобы найти истинную формулу соединения водорода и бора найдем отношение полученных молярных масс: Mgas / M(H5B2) = 54 / 27 = 2. M(H5B2) = 5 ×Ar(H) + 2 × Ar(B) = 5 ×1 + 2 × 11 = 5 + 22 = 27 г/моль. Это означает, что все индексы в формуле H5B2 следует умножить на 2. Таким образом формула вещества будет иметь вид H10B4. |
| Ответ | Формула газа — H10B4 |
| Задание | Вычислите относительную плотность по фтору углекислого газа CO2. |
| Решение | Для того, чтобы вычислить относительную плотность одного газа по другому, надо относительную молекулярную массу первого газа разделить на относительную молекулярную массу второго газа.
Относительную молекулярную массу воздуха принимают равной 29 (с учетом содержания в воздухе азота, кислорода и других газов). Следует отметить, что понятие «относительная молекулярная масса воздуха» употребляется условно, так как воздух – это смесь газов. Dair(CO2) = Mr(CO2) / Mr(F2); Dair(CO2) = 44 / 38 = 1,16. Mr(CO2) = Ar(C) + 2 ×Ar(O) = 12 + 2 × 16 = 12 + 32 = 44. |
| Ответ | Относительная плотность по фтору углекислого газа равна 1,16. |











