Плотность этилового спирта
Плотность этилового спирта и другие его физические свойства
Безводный (абсолютный) спирт кипит при 78,37oС. Получаемый в промышленности спирт-ректификат представляет собой смесь 95,5% этанола и 4,4% воды, которая кипит при 78,37oС (смеси определенного состава, кипящие при постоянной температуре, называют азеотропными смесями).
Основные константы этилового спирта приведены в таблице ниже.
Таблица 1. Физические свойства и плотность этилового спирта.
|
Плотность, г/см3 |
0,7893 |
|
Температура плавления, oС |
-114,3 |
|
Температура кипения, oС |
78,4 |
|
Молярная масса, г/моль |
46,069 |
Прием внутрь даже небольших количеств этанола понижает восприимчивость органов чувств, вызывает сильное поражение центральной нервной системы.
Химический состав и строение молекулы этилового спирта
Химический состав этилового спирта можно изобразить при помощи эмпирической (C2H5OH) и рациональной (CH3-CH2-OH) формул (рис. 1).
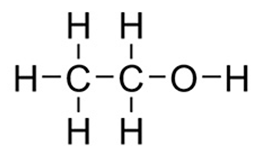
Рис. 1. Строение молекулы этилового спирта
Атом кислорода в молекуле этанола обладает большой электроотрицательностью и оттягивает на себя электронную плотность σ-связей связанных с ним атомов, в частности атома водорода. Связь O-H в молекуле этилового спирта сильно поляризована CH3-CH2→O←H. Электронная плотность в атоме водорода оказывается пониженной. Поэтому он может взаимодействовать с неподеленной парой электронов атома кислорода другой молекулы этанола. Между двумя молекулами возникает нековалентная водородная связь. Связанные между собой водородными связями молекулы этилового спирта образуют ассоциаты.
Краткая характеристика химических свойств и плотность этилового спирта
Этанол является представителем одноатомных спиртов.
За счет присутствия в воздухе кислорода, который способен выступать в роли окислителя, этиловый спирт сгорает на воздухе (светло-голубое пламя) с образованием углекислого газа и воды:
C2H5OH + 3O2 = 2CO2 + 3H2O.
За счет наличия в молекуле этанола кислотного центра он взаимодействует со щелочными, а также некоторыми щелочноземельными металлами и их гидридами с образованием солеподобных соединений – алкоголятов:
2C2H5OH + 2K = 2C2H5OK + H2;
C2H5OH + NaH = C2H5ONa + H2.
Этиловый спирт вступает в реакции нуклеофильного замещения с галогенводородными кислотами:
C2H5OH + HCl = C2H5Cl + H2O.
При взаимодействии этанола с альдегидами образуются ацетали, с карбоновыми кислотами – сложные эфиры:
C2H5OH + R-COH = R-CH(OH)-O-C2H5;
C2H5OH + R-COOH = R-COOC2H5 + H2O.
В присутствии водоотнимающих реагентов и при нагревании до температуры выше 120oС этиловый спирт подвергается дегидратации:
2C2H5OH = C2H5-O- C2H5 + H2O (H2SO4 (conc), 120oC);
CH3-CH2-OH = CH2=CH2 + H2O (H2SO4 (conc), Al2O3, 350-500oC).
Примеры решения задач
| Задание | Вычислите плотность по метану смеси, состоящей из 15 л аргона и 35 л криптона. Рассчитайте объемные доли газов в смеси. |
| Решение | Найдем объемные доли веществ в смеси:
φ = Vgas / Vmixture_gas; φ (Ar) = V(Ar) / Vmixture_gas; φ (Ar) = 15 / (15 + 35) = 15 / 50 = 0,3. φ (Kr) = V(Kr) / Vmixture_gas; φ (Kr) = 35 / (15 + 35) = 35 / 50 = 0,7. Объемные доли газов будут совпадать с молярными, т.е. с долями количеств веществ, это следствие из закона Авогадро. Найдем условную молекулярную массу смеси: Mrconditional (mixture) = φ (Ar) ×Mr(Ar) + φ (Kr) ×Mr(Kr); Mrconditional (mixture) = 0,3 × 40 + 0,7 ×84 = 12 + 58,8 = 70,8. Найдем относительную плотность смеси по метану: DCH4(mixture) = Mrconditional (mixture) / Mr(CH4); DCH4(mixture) = 70,8 / 16 = 4,425. |
| Ответ | Относительная плотность смеси аргона и криптона по метану равна 4,425. |
| Задание | Определите плотность по водороду смеси кислорода и оксида углерода (IV), если объем первого газа в смеси равен 150 л, а второго – 350 л. |
| Решение | Найдем объемные доли веществ в смеси:
φ = Vgas / Vmixture_gas; φ (O2) = V(O2) / Vmixture_gas; φ (O2) = 150 / (150 + 350) = 150 / 500 = 0,3. φ (CO2) = V(CO2) / Vmixture_gas; φ (CO2) = 350 / (150 + 350) = 350 / 500 = 0,7. Объемные доли газов будут совпадать с молярными, т.е. с долями количеств веществ, это следствие из закона Авогадро. Найдем условную молекулярную массу смеси: Mrconditional (mixture) = φ (O2) ×Mr(O2) + φ (CO2) ×Mr(CO2); Mrconditional (mixture) = 0,3 ×32 + 0,7 ×44 = 9,6 + 30,8 = 40,4. Найдем относительную плотность смеси по метану: DH2(mixture) = Mrconditional (mixture) / Mr(H2); DH2(mixture) = 40,4 / 2 = 20,2. |
| Ответ | Относительная плотность смеси газов кислорода и оксида углерода (IV) по водороду равна 20,2. |











