Строение атома фосфора
Общие сведения о строении атома фосфора
Относится к элементам p-семейства. Неметалл. Обозначение – P. Порядковый номер – 15. Относительная атомная масса – 30,974 а.е.м.
Электронное строение атома фосфора
Атом фосфора состоит из положительно заряженного ядра (+15), внутри которого есть 15 протонов и 16 нейтронов, а вокруг, по трем орбитам движутся 15 электронов.
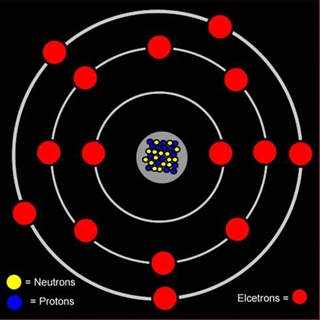
Рис.1. Схематическое строение атома фосфора.
Распределение электронов по орбиталям выглядит следующим образом:
+15 P)2)8)5;
1s22s22p63s23p3.
Внешний энергетический уровень атома фосфора содержит 5 электронов, которые являются валентными. Энергетическая диаграмма основного состояния принимает следующий вид:
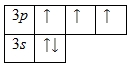
Каждый валентный электрон атома фосфора можно охарактеризовать набором из четырех квантовых чисел: n (главное квантовое), l (орбитальное), ml (магнитное) и s (спиновое):
|
Подуровень |
n |
l |
ml |
s |
|
s |
3 |
0 |
0 |
+1/2 |
|
s |
3 |
0 |
0 |
-1/2 |
|
p |
3 |
1 |
-1 |
+1/2 |
|
p |
3 |
1 |
0 |
+1/2 |
|
p |
3 |
1 |
1 |
+1/2 |
Наличие трех неспаренных электронов свидетельствует о том, что степень окисления фосфора равна +3. Так как на третьем уровне есть вакантные орбитали 3d-подуровня, то для атома фосфора характерно наличие возбужденного состояния:
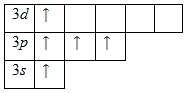
Именно поэтому для фосфора также характерна степень окисления +5.
Примеры решения задач
| Задание | Определите число нейтронов в ядре изотопа титана с массовым числом 48. |
| Решение | Массовое число А указывает суммарное число протонов Z и нейтронов в ядре атома любого элемента:
A= Z + n. Атом титана имеет порядковый номер 22, следовательно, количество протонов в ядре равно 22 (Z=22). Тогда число нейтронов в ядре атома титана определим по формуле: n= A- Z =.48 -22 = 26. |
| Ответ | n = 26 |
| Задание | Элемент состоит из двух изотопов в соотношении 2:3. Ядро первого изотопа содержит 10 протонов и 10 нейтронов. Определите атомную массу второго изотопа, если средняя относительная масса элемента равна 21,2. В ответе укажите на сколько нейтронов больше в ядре атома второго изотопа. |
| Решение | Относительная атомная масса первого изотопа равна:
A1 = Z +n = 10 + 10 = 20 а.е.м. Относительную атомную массу второго изотопа обозначим через A2. Средняя относительная атомная масса элемента определяется суммой масс его изотопов с учетом их количества. Составим уравнение: Aср ×5 = A1 ×2 + A2 ×3; 21,5 ×5 = 20 ×2 + A2 ×3; A2 = 22 а.е.м. В ядре атома второго изотопа 10 протонов, следовательно, число, нейтронов будет равно n= A- Z =.22 — 10= 12. По условию задачи в ядре атома первого изотопа было 10 нейтронов. Значит, ядро атома второго изотопа содержит на два нейтрона больше, чем ядро первого изотопа. |
| Ответ | Относительная атомная масса второго изотопа равна 22 а.е.м. |











