Строение атома серы
Общие сведения о строении атома серы
Относится к элементам p-семейства. Неметалл. Элементы-неметаллы, входящие в эту группу, носят общее название халькогены. Обозначение – S. Порядковый номер – 16. Относительная атомная масса — 32,064 а.е.м.
Электронное строение атома серы
Атом серы состоит из положительно заряженного ядра (+16), состоящего из 16 протонов и 16 нейтронов, вокруг которого по 3-м орбитам движутся 16 электронов.
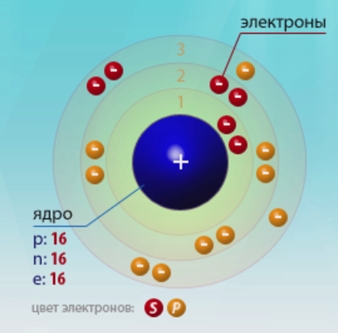
Рис.1. Схематическое строение атома серы.
Распределение электронов по орбиталям выглядит следующим образом:
+16S)2)8)6;
1s22s22p63s23p4.
На внешнем энергетическом уровне атома серы находится шесть электронов, все они считаются валентными. Энергетическая диаграмма принимает следующий вид:
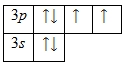
Наличие двух неспаренных электронов свидетельствует о том, что сера способна проявлять степень окисления +2. Также возможно несколько возбужденных состояний из-за наличия вакантной 3d-орбитали. Сначала распариваются электроны 3p -подуровня и занимают свободные d-орбитали, а после – электроны 3s-подуровня:
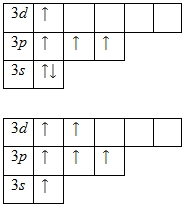
Этим объясняется наличие у серы ещё двух степеней окисления: +4 и +6.
Примеры решения задач
| Задание | Средняя относительная атомная масса природного хлора равна 35,45. Определите массовые доли двух изотопов хлора, если их массовые числа равны 35 и 37. |
| Решение | Изотопы – это атомы одного и того же химического элемента, имеющие разные массовые числа (одинаковое число протонов, но разное – нейтронов). Примем за х число атомов изотопа хлора 35Cl в каждых ста атомах природного хлора, тогда число атомов изотопа 37Cl будет равно (100-х). Масса атомов изотопа 35Cl будет равна 35х, а 37Cl – 37×(100-х). Составим уравнение:
35х + 37×(100-х) = 35,45×100%. Найдем х: 35х + 3700 — 37х = 3545; 2х = 155; х = 77,5. Значит содержание изотопа 35Cl в природном хлоре равно 77,5%. Тогда, содержание изотопа 37Cl: 100-77,5 = 22,5%. |
| Ответ | Содержание изотопа 35Cl в природном хлоре равно 77,5%, а 37Cl — 22,5%. |
| Задание | Природный магний состоит из изотопов 2412Mg (78,6%), 2512Mg (10,1%) и 2612Mg (11,3%). Определите относительную атомную массу магния. |
| Решение | Средняя относительная масса изотопов рассчитывается по формуле:
Ar = (Ar1 × ω1 + Ar2 × ω2 + Ar3 × ω3)/100. Рассчитываем среднюю относительную атомную массу магния: Ar(Mg) = (24 × 78,6 + 25 × 10,1 + 26 × 11,3)/100; Ar(Mg) = (1886,4 + 252,5 + 293,8)/100 = 24,327а.е.м. |
| Ответ | Ar(Mg) = 24,327 а.е.м. |











