Формулы сульфатов
Определение и формулы сульфатов
Серная кислота представляет собой двухосновную кислоту, которая подвергается ступенчатой диссоциации:
H2SO4 ↔ H+ + HSO4—;
HSO4— ↔ H+ + SO42-,
тем самым образуя соли – сульфаты – двух видов:
— сульфаты – замещены все атомы водорода в серной кислоте, например, K2SO4 –сульфат калия, (NH4)2SO4 – сульфат аммония;
— гидросульфаты – замещен один атом водорода в серной кислоте, например, KHSO4–гидросульфат калия, NH4HSO4 – гидросульфат аммония.
Химические формулы сульфатов
Химические формулы сульфатов рассмотрим на примере калиевых солей серной кислоты: K2SO4 –сульфата калия и KHSO4–гидросульфата калия. Химическая формула показывает качественный и количественный состав молекулы (сколько и каких атомов входит в конкретное соединение) По химической формуле можно вычислить молекулярную массу сульфидов (Ar(K) = 39 а.е.м., Ar(H) = 1 а.е.м., Ar(S) = 32 а.е.м., Ar(O) = 16 а.е.м.):
Mr(K2SO4) = 2×Ar(K) + Ar(S) + 4×Ar(O);
Mr(K2SO4) = 2×39 + 32 + 4×16 = 78 + 32 + 64= 174.
Mr(KHSO4) = Ar(K) + Ar(H) + Ar(S) + 4×Ar(O);
Mr(KHSO4) = 39 + 1 + 32 + 4×16= 72 + 64 = 136.
Графические (структурные) формулы сульфатов
Структурная (графическая) формула является более наглядной. Рассмотрим структурные формулы сульфатов на примере все тех же калиевых солей сероводородной кислоты: K2SO4 –сульфата калия и KHSO4–гидросульфата калия.
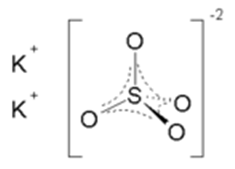
Рис. 1. Структурная формула сульфата калия.
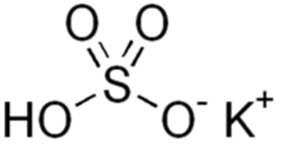
Рис. 2. Структурная формула гидросульфата калия.
Ионная формула
Сульфаты представляют собой соли разного типа (средние и кислые), каждая из которых способна диссоциировать в водном растворе:
K2SO4 ↔ 2K+ + SO42-;
KHSO4 ↔ K+ + HSO4—.
Примеры решения задач
| Задание | Найдите химическую формулу вещества, в состав которого входит 5 массовых частей кальция и 4 массовых части серы. |
| Решение | Для того, чтобы узнать, в каких отношениях находятся химические элементы в составе молекулы необходимо найти их количество вещества. Известно, что для нахождения количества вещества следует использовать формулу:
n = m / M. Найдем молярные массы кальция и серы (значения относительных атомных масс, взятых из Периодической таблицы Д.И. Менделеева, округлим до целых чисел). Известно, что M = Mr, значит M(Ca)= 40 г/моль, а М(S) = 32 г/моль. Тогда, количество вещества этих элементов равно: n (Ca) = m (Ca) / M (Ca); n (Ca) = 5 / 40 = 0,125 моль. n (S) = m (S) / M (S); n (S) = 4 / 32 = 0,125 моль. Найдем мольное отношение: n(Ca) :n(O) = 0,125 : 0,125= 1 : 1, т.е. формула соединения кальция с серой имеет вид CaS.Это сульфид кальция. |
| Ответ | CaS |
| Задание | Найдите химическую формулу вещества, в состав которого входит 31 массовая часть фосфора и 40 массовых частей кислорода. |
| Решение | Для того, чтобы узнать, в каких отношениях находятся химические элементы в составе молекулы необходимо найти их количество вещества. Известно, что для нахождения количества вещества следует использовать формулу:
n = m / M. Найдем молярные массы фосфора и кислорода (значения относительных атомных масс, взятых из Периодической таблицы Д.И. Менделеева, округлим до целых чисел). Известно, что M = Mr, значит M(P)= 31 г/моль, а М(O) = 16 г/моль. Тогда, количество вещества этих элементов равно: n (P) = m (P) / M (P); n (P) = 31 / 31 = 1 моль. n (O) = m (O) / M (O); n (O) = 40 / 16 = 2,5 моль. Найдем мольное отношение: n(P) :n(O) = 1 : 2,5= 2 : 5, т.е. формула соединения кальция с серой имеет вид P2O5.Это оксид фосфора (V). |
| Ответ | P2O5 |











