Молярная масса кислорода
Молярная масса кислорода
M = m / n
Единицей измерения молярной массы является г/моль или кг/кмоль. Молярная масса вещества в граммах численно равна его молекулярной (атомной) массе, выраженной в атомных единицах массы:
M = Ar.
Относительная атомная масса атомарного кислорода равна 15,99903 а.е.м. Его относительная молекулярная масса будет равна 15,99903, а молярная масса:
M(O) = Mr (O) × 1 моль = 15,99903 г/моль.
Известно, что молекула кислорода двухатомна – O2, тогда, относительная атомная масса молекулы кислорода будет равна:
Ar(O2) = 15,99903 × 2 = 31,99806а.е.м.
Относительная молекулярная масса молекулы кислорода будет равна 31,99806, а молярная масса:
M(O2) = Mr (O2) × 1 моль = 31,99806 г/моль или просто 32 г/моль.
Кислород представляет собой газ без цвета и запаха (схема строения атома представлена на рис. 1), плохо растворимый в воде с очень низкими значениями температур плавления(-218,9oC) и кипения (-183oC).
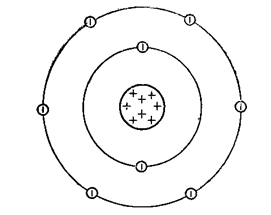
Рис. 1. Строение атома кислорода.
Известно, что в природе кислород может находиться в виде трех изотопов 16O (99,76%), 17O (0,04%) и 18O (0,2%). Эти изотопы характеризуются различным содержанием нейтронов в ядре атома, а значит и молярной массой. В первом случае она будет равна 16 г/моль, во втором – 17 г/моль, а в третьем – 18 г/моль.
Молярную массу газа можно рассчитать, как произведение его плотности по отношению к любому другому газу на молекулярную массу последнего. Под плотностью понимают отношение массу определенного объема данного газа к массе такого же объема другого газа (при одинаковых температуре и давлении), молекулярная масса которого известна.
Молекулярную массу вещества в газообразном состоянии также можно рассчитать, зная его молярный объем: найти объем (н.у.), занимаемый определенной массой данного вещества, а затем вычислить массу 22,4 л этого вещества при этих же условиях.
Кроме этих способов, чтобы определить молярную массу газа, возможно использование уравнения состояния идеального газа (уравнение Менделеева-Клапейрона), однако это метод является наименее точным из всех перечисленных.
Примеры решения задач
| Задание | Рассчитайте массу кислорода, который будет получен при разложении оксида ртути (II) массой 65,1 г. |
| Решение | Запишем уравнение химической реакции разложения оксида ртути (II):
2HgO = 2Hg + 2O2. Найдем количество вещества оксида ртути (II), вступившего в реакцию (молярная масса равна 217 г/моль): n = m / M; n(HgO) = m(HgO) / M(HgO); n(HgO) = 65,1 / 217 = 0,3моль. Согласно уравнению реакции n(HgO) : n(O2) = 1:1, т.е. n(HgO) = n(O2) = 0,3 моль. Рассчитаем массу выделившегося кислорода (молярная масса равна 32 г/моль): m = n × M; m(O2) = n(O2) × M(O2); m(O2) = 0,3 × 32 = 9,6 г. |
| Ответ | Масса кислорода равна 9,6 г |
| Задание | В каком случае будет получено больше кислорода: при разложении 5 г хлората калия или при разложении 5 г перманганата калия? |
| Решение | Запишем уравнения реакций разложения хлората калия и перманганата калия:
2KClO3 = 2KCl + 3O2↑ (1); 2KMnO4 = K2MnO4 + MnO2 + O2↑ (2). Найдем количество вещества хлората калия (молярная масса равна – 122,55 г/моль): n = m / M; n(KClO3) = m(KClO3) / M(KClO3); n(KClO3) = 5 / 122,55= 0,04 моль. Согласно уравнению реакции (1) n(KClO3) : n(O2) = 2:3; n(O2) = 3/2×n(KClO3); n(N2) = 3/2×0,04 = 0,06моль. Рассчитаем массу выделившегося кислорода (молярная масса равна 32 г/моль): m = n × M; m(O2) = n(O2) × M(O2); m(O2) = 0,06 × 32 = 1,92 г. Найдем количество вещества перманганата калия (молярная масса равна – 158,03 г/моль): n = m / M; n(KMnO4) = m(KMnO4) / M(KMnO4); n(KMnO4) = 5 / 158,03= 0,03моль. Согласно уравнению реакции (2) n(KMnO4) : n(O2) = 2:1; n(O2) = 1/2×n(KMnO4); n(N2) = 1/2×0,03 = 0,015моль. Рассчитаем массу выделившегося кислорода (молярная масса равна 32 г/моль): m = n × M; m(O2) = n(O2) × M(O2); m(O2) = 0,015 × 32 = 0,48 г. |
| Ответ | Масса кислорода, выделяющегося при разложении 5 г хлората калия больше (1,92 г), чем при разложении аналогичного количества перманганата калия (0,48 г). |











