Формула сульфата бария
Определение и формула сульфата бария
Не растворяется в воде. Кристаллогидратов не образует. Малореакционноспособный, не реагирует с кислотами (кроме концентрированной серной). Восстанавливается углеродом при спекании.

Рис. 1. Сульфат бария. Внешний вид.
Химическая формула сульфата бария
Химическая формула сульфата бария BaSO4. Она показывает, что в состав данной молекулы входят один атом бария (Ar = 137а.е.м.), один атом серы (Ar = 32 а.е.м.) и четыре атома кислорода (Ar = 16 а.е.м.). По химической формуле можно вычислить молекулярную массу сульфата бария:
Mr(BaSO4) = Ar(Ba) + Ar(S) + 4×Ar(O);
Mr(BaSO4) = 137 + 32 + 4×16 = 169 + 64 = 233.
Структурная (графическая) формула сульфата бария
Структурная (графическая) формула сульфата бария является более наглядной. Она показывает то, как связаны атомы между собой внутри молекулы:
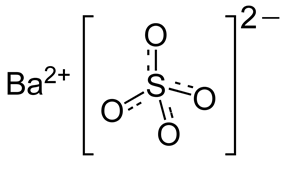
Ионная формула
Сульфат бария представляет собой электролит, который диссоциирует на ионы в водном растворе согласно следующему уравнению реакции:
BaSO4 ↔ Ba2+ + SO42-.
Примеры решения задач
| Задание | В оксиде хлора массой 3,66 г содержится 1,42 г хлора. Определите формулу оксида хлора. |
| Решение | Для того, чтобы узнать, в каких отношениях находятся химические элементы в составе молекулы необходимо найти их количество вещества. Известно, что для нахождения количества вещества следует использовать формулу:
n = m / M. Найдем молярные массы хлора и кислорода (значения относительных атомных масс, взятых из Периодической таблицы Д.И. Менделеева, округлим до целых чисел). Известно, что M = Mr, значит M(Cl)= 35,5 г/моль, а М(O) = 16 г/моль. Определим массу кислорода в составе оксида хлора: m(O) = m (ClxOy) – m(Cl); m(O) = 3,66 – 1,42 = 2,24 г. Тогда, количество вещества этих элементов равно: n (Cl) = m (Cl) / M (Cl); n (Cl) = 1,42 / 35,5 = 0,04 моль. n (O) = m (O) / M (O); n (O) = 2,24 / 16 = 0,14 моль. Найдем мольное отношение: n(Cl) :n(O)= 0,04 : 0,14 = 1 : 3,5 = 2 : 7, т.е. формула оксида хлора имеет вид Cl2O7. |
| Ответ | Cl2O7 |
| Задание | Химический анализ образца органического вещества массой 3,16 г показал, что в его состав входят 0,92 г углерода, 0,12 г водорода, 0,8 г кальция, а остальное – кислород. Составьте формулу этого соединения. |
| Решение | Для того, чтобы узнать, в каких отношениях находятся химические элементы в составе молекулы необходимо найти их количество вещества. Известно, что для нахождения количества вещества следует использовать формулу:
n = m / M. Найдем молярные массы углерода водорода, кальция и кислорода (значения относительных атомных масс, взятых из Периодической таблицы Д.И. Менделеева, округлим до целых чисел). Известно, что M = Mr, значит M(С)= 12 г/моль, M(H) = 1 г/моль, M(Ca) = 40 г/моль, а М(O) = 16 г/моль. Определим массу кислорода в составе вещества: m(O) = m (CxHyCazOw) – m(C)– m(H) – m(Ca); m(O) = 3,16 – 0,92 – 0,12 – 0,8 = 1,32 г. Тогда, количество вещества этих элементов равно: n (C) = m (C) / M (C); n (C) = 0,92 / 12 = 0,08 моль. n (H) = m (H) / M (H); n (H) = 0,12 / 1 = 0,12 моль. n (Ca) = m (Ca) / M (Ca); n (Ca) = 0,8 / 40 = 0,02 моль. n (O) = m (O) / M (O); n (O) = 1,32 / 16 = 0,0825 моль. Найдем мольное отношение: n(C) :n(H) : n(Ca) :n(O)=0,08 : 0,12 : 0,02 : 0,0825 = 4 : 6 : 1 : 4, т.е. формула соединения углерода, водорода, кальция и кислорода имеет вид C4H6CaO4или (CH3COO)2Ca. Это ацетат кальция. |
| Ответ | (CH3COO)2Ca |











