Электронная конфигурация фосфора
Задание по теме фосфор. Подскажите, электронная конфигурация фосфора каким образом. Кроме этого надо указать число электронов на внешнем энергетическом уровне. Есть ли среди них неспаренные?
Фосфор – неметалл, расположен в VA группе в третьем периоде Периодической таблицы Д.И. Менделеева. Относится к химическим элементам р— семейства. Для фосфора характерно явление аллотропии, т.е. существование в природе виде нескольких простых веществ – аллотропных видоизменений: белый, красный и черный фосфор. Иногда говорят о желтом и металлическом фосфоре. Данные модификации отличаются не только по внешнему виду, физическим свойствам, но и химической активности.
Обозначение фосфора в Периодической таблице Д.И. Менделеева – P. Порядковый номер – 15, значит заряд ядра атома равен (+15). В ядре атома фосфора содержится 15 протонов и 16 нейтронов (массовое число равно 31). В атоме фосфора есть три энергетических уровня, на которых находятся 15 электронов. Электронная конфигурация основного состояния имеет вид:
![]() .
.
Электронно-графическая схема выглядит следующим образом:
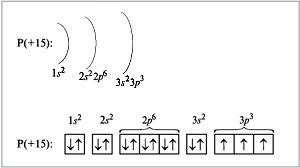
На внешнем энергетическом уровне находится 5 электронов, из которых три неспаренных. Однако, из-за наличия незаполненных орбиталей 3d-валентного уровня, при сильном возбуждении электроны 3s-подуровня могут распариваться и один из них способен занимать вакантную орбиталь 3d-подуровня. Т.е. число валентных электронов в атоме фосфора в возбужденном состоянии равно пяти.
Проявляет валентности равные III и V.










