Валентность титана
Общие сведения о валентности титана
В Виде простого вещества титан представляет собой серебристо-белый металл. Относится к легким металлам. Тугоплавок. Плотность – 4,50 г/см3. Температуры плавления и кипения равны 1668oС и 3330oС, соответственно.
Титан коррозионно-устойчив при на воздухе при обычной температуре, что объясняется наличием на его поверхности защитной пленки состава TiO2. Химически устойчив во многих агрессивных средах (растворы сульфатов, хлоридов, морской воды и т.д.).
Валентность титана в соединениях
Титан находится в четвертом периоде в IVB группе Периодической таблицы Д.И. Менделеева. Порядковый номер равен 22. В ядре атома титана содержится 22 протона и 26 нейтронов (массовое число равно 48). В атоме титана есть четыре энергетических уровня, на которых находятся 22 электрона (рис. 1).

Рис. 1. Строения атома титана.
Электронная формула атома титана в основном состоянии имеет следующий вид:
1s22s22p63s23p63d24s2.
А энергетическая диаграмма (строится только для электронов внешнего энергетического уровня, которые по-другому называют валентными):
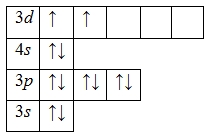
Наличие двух неспаренных электронов свидетельствует о том, что титан в своих соединениях может проявлять валентность II (TiIIO).
Атом титана способен переходить в возбужденное состояние: электроны 4s-подуровня распариваются и один из них занимает вакантную орбиталь 3d-подуровня:
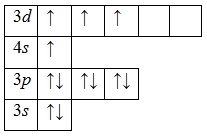
Наличие четырех неспаренных электронов свидетельствует о том, что титан также проявляет валентность IV в своих соединениях (TiIVO2, TiIVF4).
Известно, что у титана есть валентность III (TiIII2O3, TiIIICl3).
Примеры решения задач
| Задание | Рассчитайте массу титана, полученного термическим разложением йодида титана (IV)TiI4, на образование которого затрачен йод массой 10,16 г. |
| Решение | Запишем уравнение реакции термического разложения йодида титана (IV):
TiI4 = Ti +2I2. Найдем количество вещества йода, вступившего в реакцию (молярная масса – 254 г/моль): n = m / M; n (I2) = m (I2) / M (I2); n (I2) = 10,16 / 254 = 0,04 моль. Согласно уравнению реакции n(Ti) :n(I2) = 1:2, значит, n(Ti) = ½ ×n (I2) = ½ ×0,04 = 0,02 моль. Тогда, масса титана будет равна (молярная масса – 48 г/моль): m = n × M; m (Ti) = n (Ti) × M (Ti); m (Ti) = 0,02 × 48 = 0,96 г. |
| Ответ | Масса титана равна 0,96 г. |
| Задание | Вычислите количество теплоты, выделяющейся при восстановлении хлорида титана (IV) массой 47,5 г магнием. Термохимическое уравнение реакции имеет следующий вид:
TiCl4 + 2Mg = Ti + 2MgCl2 =477 кДж. |
| Решение | Запишем еще раз термохимическое уравнение реакции:
TiCl4 + 2Mg = Ti + 2MgCl2 =477 кДж. Согласно уравнению реакции, в неё вступили 1 моль хлорида титана (IV) и 2 моль магния. Рассчитаем массу хлорида титана (IV) по уравнению, т.е. теоретическую массу (молярная масса – 190 г/моль): m = n × M; mtheor (TiCl4) = n (TiCl4) × M (TiCl4); mtheor (TiCl4) = 1 × 190 = 190 г. Составим пропорцию: mprac(TiCl4)/mtheor (TiCl4) = Qprac/Qtheor. Тогда, количество теплоты, выделяющейся при восстановлении хлорида титана (IV) магнием равно: Qprac = Qtheor × mprac(TiCl4)/mtheor; Qprac = 477 × 47,5/ 190 = 119,25 кДж. |
| Ответ | Количество теплоты равно 119,25 кДж. |











