Валентность неона
Общие сведения о валентности неона
Основное отличие неона от гелия – большая поляризуемость атома, склонность к образованию межмолекулярных связей, несколько большая растворимость и способность адсорбироваться.
Валентность неона в соединениях
Ядро атома неона содержит 10 протонов и 10 нейтронов (массовое число равно 20-ти). В атоме неона есть два энергетических уровня, на которых находятся 10 электронов (рис. 1).
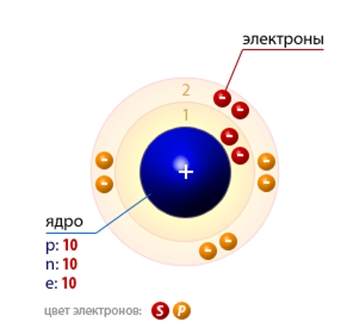
Рис. 1. Строение атома неона.
Электронная формула атома неона в основном состоянии выглядит следующим образом:
1s22s22p6.
А энергетическая диаграмма (строится только для электронов внешнего энергетического уровня, которые по-другому называют валентными):
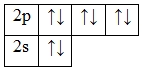
Поскольку на s-подуровне может содержаться не более 2-х электронов, а на p-подуровне – не больше 6-ти электронов, то внешний энергетический уровень неона является завершенным. В этой связи неон является малоактивным химическим элементом и выделен в группу инертных газов. Т.е., можно сказать, что валентность гелия равна нулю.
Как и гелий, неон при сильном возбуждении атомов образует молекулярные ионы типа Ne2+:
σs2σs*2σz2πx,y4πx,y*4πz*1.
Примеры решения задач
| Задание | Для какого из перечисленных элементов характерно всего одно значение валентности: 1) углерод; 2) хлор; 3) фосфор; 4) фтор. |
| Ответ | Среди перечисленных выше химических элементов всего одна валентность характерна только для фтора (I). Все остальные элементы проявляют, как минимум, по две валентности. |
| Задание | Высшая валентность увеличивается в ряду элементов: 1) C-Si-Ge; 2) Cl –Br-I; 3) N-C-B; 4) Al-Si-P. |
| Решение | Высшую валентность химического элемента можно определить с помощью Периодической таблицы Д.И. Менделеева. Она равна номеру группы, в которой расположен элемент. Увеличение значения высшей валентности для при переходе от одного элемента к другому увеличивается в ряду алюминий, кремний, фосфор – вариант 4. |
| Ответ | Вариант 4. |











