Валентность кислорода
Общие сведения о валентности кислорода
Природный кислород состоит из трех стабильных изотопов 16O (99,76%), 17O (0,04%) и 18O (0,2%).
Наиболее устойчива двухатомная молекула кислорода O2. Она парамгнитна и слабо поляризуется. Температуры плавления (-218,9oС) и кипения (-183oС) кислорода очень низкие. Кислород плохо растворяется в воде. При нормальных условиях кислород представляет собой газ без цвета и запаха.
Жидкий и твердый кислород притягивается магнитом, т.к. его молекулы парамагнитны. Твердый кислород синего цвета, а жидкий – голубого. Окраска обусловлена взаимным влиянием молекул.
Кислород существует в виде двух аллотропных модификаций – кислорода O2 и озона O3.
Валентность кислорода в соединениях
Кислород — восьмой по счету элемент Периодической таблицы Д.И. Менделеева. Он находится во втором периоде во VIA группе. В ядре атома кислорода содержится 8 протонов и 8 нейтронов (массовое число равно 16). В атоме кислорода есть два энергетических уровня, на которых находятся 8 электронов (рис. 1).
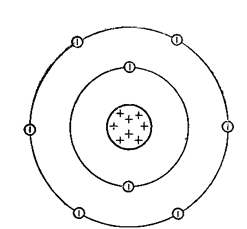
Рис. 1. Строения атома кислорода.
Электронная формула атома кислорода в основном состоянии имеет следующий вид:
1s22s22p4.
А энергетическая диаграмма (строится только для электронов внешнего энергетического уровня, которые по-другому называют валентными):
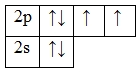
Наличие двух неспаренных электронов свидетельствует о том, что кислород может проявлять валентность II в своих соединения (CaOII, Na2OII, Al2OII3, Cl2OII7, H2OII2 и т.д.).
Так как на 2 энергетическом слое нет подуровней кроме 2s и 2p, которые уже заняты электронами, возбужденного состояния у кислорода нет.
Примеры решения задач
| Задание | Валентность V атом азота имеет в соединении: 1)KNO3; 2) KNO2; 3) NO; 4) Ca(NO2)2. |
| Решение | Все перечисленные выше соединения, за исключением вещества под номером 3 (оксид) относятся к классу средних солей. Валентность азота в данном случае определяют следующим образом: находят число атомов кислорода, вычисляют общее число единиц валентности для кислорода, вычисляют общее число единиц валентности для металла, находят разность двух последних величин и делят её на число атомов азота.
Рассмотрим на примере нитрата калия (KNO3). Общее число атомов кислорода равно 3 (см. нижний индекс). Общее число единиц валентности для кислорода равно: 3 × 2 = 6 (валентность кислорода равна II). общее число единиц валентности для металла равно: 1 (нижний индекс калия) × 1 = 1 (калий элемент IA группы, для которых валентность равна номеру и является постоянной величиной). Разность общих чисел единиц валентностей кислорода и калия равна: 6-1 = 5. Значит валентность азота равная V. Это и есть правильный ответ. |
| Ответ | Вариант ответа 1. |
| Задание | Укажите, чему равны валентности элементов, входящих в состав перечисленных соединений: P2O5, CaO, SO3, N2O5, BaO, CO2, Fe2O3 и CO. |
| Ответ | Определение валентностей элементов в химическом соединении стоит начинать с указания валентности известного элемента. Все перечисленные выше соединения относятся к классу оксидов. Валентность кислорода в оксидах всегда равна II. Рассмотрим на примере первого вещества. Запишем его формулу и укажем римскими цифрами валентность известного элемента:
P2OII5. Находим наименьшее кратное чисел единиц валентностей. Для этого умножаем значение валентности кислорода на количество атомов данного элемента в соединении (5): 2 × 5 = 10. Чтобы определить валентность фосфора поделим наименьшее кратное чисел единиц валентностей на количество атомов фосфора в соединении (2): 10 / 2 = 5. Это означает, что валентность фосфора равна V: PV2OII5. Аналогичным образом определяем валентности элементов в других соединениях: CaIIOII, SIIIOII3, NV2OII5, BaIIOII, CIVOII2, FeIII2OII3 и CIIOII. |











