Валентность фосфора
Общие сведения о валентности фосфора
Фосфор образует несколько аллотропических изменений: белый, красный и черный фосфор.
В чистом виде белый фосфор совершенно бесцветен и прозрачен; технический белый фосфор окрашен в желтоватый цвет и по внешнему виду похож на воск. Плотность 1,83 г/см3. На холоду белый фосфор хрупок, но при температуре выше 15oС становится мягким и легко режется ножом. На воздухе он легко окисляется, вследствие чего светится в темноте. Имеет молекулярную кристаллическую решетку в узлах которой находятся тетраэдрические молекулы P4. Ядовит.
Красный фосфор состоит из нескольких форм, являющихся полимерными веществами, состав которых до конца не изучен. Медленно окисляется на воздухе, не светится в темноте, неядовит. Плотность 2,0-2,4г/см3. При нагревании сублимируется. При охлаждении паров красного фосфора получается белый фосфор.
Черный фосфор образуется из белого путем его нагревания под высоким давлением при 200-220oС. По внешнему виду похож на графит, жирный на ощупь. Плотность – 2,7г/см3. Полупроводник.
Валентность фосфора в соединениях
Фосфор — пятнадцатый по счету элемент Периодической таблицы Д.И. Менделеева. Он находится в третьем периоде в VA группе. В ядре атома фосфора содержится 15 протонов и 16 нейтронов (массовое число равно 31). В атоме фосфора есть три энергетических уровня, на которых находятся 15 электронов (рис. 1).
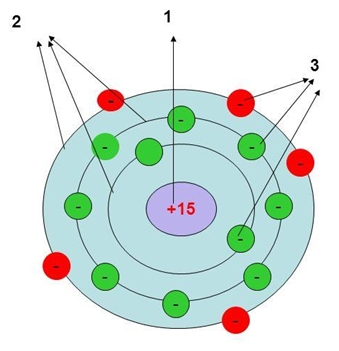
Рис. 1. Строения атома фосфора.
Электронная формула атома фосфора в основном состоянии имеет следующий вид:
1s22s22p63s23p3.
А энергетическая диаграмма (строится только для электронов внешнего энергетического уровня, которые по-другому называют валентными):
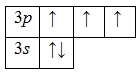
Наличие трех неспаренных электронов свидетельствует о том, что фосфор способен проявлять валентность III (PIII2O3, Ca3PIII2, PIIIH3и т.д.).
Поскольку на третьем энергетическом слое помимо 3s- и 3p-подуровней есть еще и 3d-подуровень, для атома фосфора характерно наличие возбужденного состояния: пара электронов 3s-подуровня распаривается и один из них занимает вакантную орбиталь 3d-подуровня.
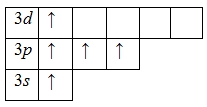
Наличие пяти неспаренных электронов свидетельствует о том, что для фосфора также характерна валентность V (PV2O5, H3PVO4, PVCl5и др.).
Примеры решения задач
| Задание | Вычислите массу фосфора, который надо сжечь в кислороде для получения оксида фосфора (V) массой 3,5 г. |
| Решение | Запишем уравнение реакции сжигания фосфора в кислороде с образованием оксида фосфора (V):
4P + 5O2 = 2P2O5. Рассчитаем количество вещества оксида фосфора (V) (молярная масса – 284 г/моль): n = m / M; n(P2O5) = m (P2O5) / M (P2O5); n (P2O5) = 3,5 / 284 = 0,01 моль. Согласно уравнению реакции n(P2O5) :n(P) = 1:2 . Тогда количество моль фосфора будет равно: n (P) = 2 × n (P2O5) = 2 × 0,01 = 0,02моль. Найдем массу фосфора (молярная масса – 31 г/моль): m = n × M; m (P) = n (P) × M (P); m (P) = 0,02 × 31 = 0,62 г. |
| Ответ | Масса фосфора равна 0,62 г. |
| Задание | Каков тип химической связи в соединениях: а) PH3; б) PCl5; в)Li3P. В полярных веществах укажите направления смещения общих электронных пар. |
| Ответ | В соединениях состава PH3 и PCl5 реализуется ковалентная полярная связь, поскольку эти вещества образованы атомами неметаллов, отличающихся по своей электроотрицательности. Поскольку значения электроотрицательности фосфора в фосфине и хлора в пентахлориде фосфора выше, чем у водорода и фосфора, соответственно, то общие электронные пары будут смещены в их сторону.
В соединении Li3P реализуется ионный тип связи. |











