Элементы с постоянной валентностью
Понятие валентность
Мерой валентности поэтому может быть число химических связей, образуемых данным атомом с другими атомами. Таким образом, в настоящее время под валентностью химического элемента обычно понимается его способность (в более узком смысле – мера его способности) к образованию химических связей. В представлении метода валентных связей числовое значение валентности соответствует числу ковалентных связей, которые образует атом.
Элементы с постоянной валентностью
Существуют элементы с т.н. постоянной валентностью (металлы IA и IIA групп, алюминий водород, фтор, кислород и т.д.), которые в своих соединениях проявляют единственную степень окисления, которая чаще всего совпадает с номером группы Периодической таблицы Д.И. Менделеева, где они расположены). Рассмотрим на примере некоторых химических элементов.
Валентность элементов главной подгруппы I группы равна единице, так ка на внешнем уровне атомы этих элементов имеют один электрон:
3Li 1s22s1

11Na 1s22s22p63s1

Валентность элементов главной подгруппы II группы в основном (невозбужденном) состоянии равна нулю, так как на внешнем энергетическом уровне нет неспаренных электронов:
4Be1s22s2

12Mg 1s22s22p63s2

При возбуждении этих атомов спаренные s-электроны разъединяются в свободные ячейки p-подуровня этого же уровня и валентность становится равной двум (II):
Be*
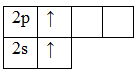
Mg*
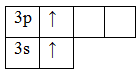
Кислород и фтор во всех соединениях проявляют постоянную валентность, равную двум (II) для кислорода и единице (I) для фтора. Валентные электроны этих элементов находятся на втором энергетическом уровне, где нет более свободных ячеек:
8O 1s22s22p4
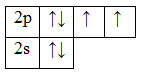
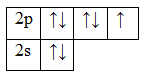
9F 1s22s22p5
Примеры решения задач
| Задание | Число неспаренных электронов в атоме бора в основном состоянии такое же, как и в атоме: 1) рубидия; 2) кремния; 3) кислорода; 4) кальция. |
| Решение | Число неспаренных электронов в атоме химического элемента чаще всего равно одному из значений валентности, которые проявляет этот элемент. Чтобы определить число неспаренных электронов в атоме бора в основном состоянии запишем электронную формулу этого элемента:
5B 1s22s22p1. На внешнем электронном уровне бора находится 3 электрона из которых только один неспаренный. Один неспаренный электрон в основном состоянии также имеет рубидий, поскольку он расположен в IA группе и на его внешнем электронном уровне находится всего один электрон, который, естественно, является неспаренным. |
| Ответ | Вариант 1 |
| Задание | Определите валентность элементов в следующих соединениях: а) NH3; б) SO2; в) CO2; г) H2S; д) P2O5. |
| Решение | Определение валентностей элементов в химическом соединении стоит начинать с указания валентности известного элемента. В варианте «а» — это водород, поскольку его валентность всегда равна I:
NHI3. Далее определяем общее число единиц валентности атомов этого элемента: 1 × 3 =3. Проставляем полученное значение справа от химического знака этого элемента, обозначая арабскими цифрами: NHI3 (3). Теперь делим общее число единиц валентности на число атомов (индекс) элемента, для которого известна валентность: 3 / 1 = 3. Поставим полученное частное (3) римской цифрой над искомым элементом как его валентность: NIIIHI3. Значит валентность элементов в соединении NH3 равна: у азота – III и у водорода – I. Аналогичным образом определяем валентности элементов в других соединениях: б) SIVOII2; в) CIVOII2; г) HI2SII; д) PV2OII5. |
| Ответ | а) NIIIHI3;б) SIVOII2; в) CIVOII2; г) HI2SII; д) PV2OII5 |











