Степень окисления в Na3N
Общие сведения об азиде натрия и степени окисления в Na3N

Рис. 1. Азид натрия. Внешний вид.
Брутто-формула – Na3N. Молярная масса равна 65,01 г/моль. Молекула азида натрия имеет вид:
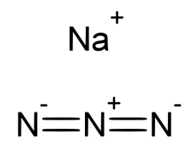
Хорошо растворяется в воде (гидролизуется по аниону). Кристаллогидратов не образует. Разлагается кислотами. Проявляет окислительно-восстановительные свойства.
Na3N, степени окисления элементов в нем
Чтобы определить степени окисления элементов, входящих в состав азида натрия, сначала необходимо разобраться с тем, для каких элементов эта величина точно известна.
Степень окисления натрия постоянна и равна номеру группы Периодической системы Д.И. Менделеева, в которой он расположен со знаком плюс (натрий – металл), т.е. (+1). Для нахождения степени окисления азота примем её значение за «х» и определим его при помощи уравнения электронейтральности:
3× (+1) + х = 0;
3 + х = 0;
x = -3.
Значит степень окисления азота в азиде натрия равна (-3):
Na+13N-3.
Примеры решения задач
| Задание | Установите соответствие между уравнением окислительно-восстановительной реакции и свойством азота, которое он проявляет в этой реакции.
|
||||||||||
| Ответ | а) В данной реакции степень окисления азота изменяется с (+2) в NO до (+4) в NO2. Так как степень окисления повысилась, то азот выступает в роли восстановителя. Вариант 2.
б) В данной реакции степень окисления азота изменяется с (-3) в NH3 до 0 в N2. Так как степень окисления повысилась, то азот выступает в роли восстановителя. Вариант 2. в) В данной реакции степень окисления азота изменяется с (-3) в NH3 до (+2) в NO. Так как степень окисления повысилась, то азот выступает в роли восстановителя. Вариант 2. г) В данной реакции степень окисления азота изменяется с 0 в N2 до (-3) в Li3N. Так как степень окисления понизилась, то азот выступает в роли окислителя. Вариант 1. |
| Задание | Степень окисления, равную (+6), атом хрома имеет в соединении: а) CrCl3; б) K2Cr2O7; в) Cr2S3; г) KCrO2. |
| Решение | Будем поочередно определять степень окисления хрома в каждом из соединений, а выберем то, в котором его степень окисления равна (+6).
а) Хлорид хрома (III) — CrCl3. Степень окисления кислотного остатка определяется числом атомов водорода, входящих в состав образующей его кислоты, указанных со знаком минус. Хлорид-ион – это кислотный остаток хлороводородной кислоты, формула которой HCl. В её составе имеется один атом водорода, следовательно, степень окисления хлора в хлорид-ионе равна (-1).Для нахождения степени окисления хрома примем её значение за «х» и определим его при помощи уравнения электронейтральности: x + 3× (-1)= 0; х– 3 = 0; x = +3. Значит степень окисления хрома в хлориде хрома (III) равна (+3). Неверный ответ. б) Дихромат калия — K2Cr2O7. Степень окисления калия постоянна и равна номеру группы в Периодической таблице Д.И. Менделеева, в которой он находится, со знаком плюс, т.е. (+1). Степень окисления кислорода в составе неорганических кислот, а, следовательно, и в составе их кислотных остатков, всегда равна (-2). Для нахождения степени окисления хрома примем её значение за «х» и определим его при помощи уравнения электронейтральности: 2×(+1) + 2×х + 7×(-2) = 0; 2 + 2х — 14 = 0; 2х — 12 = 0; 2х =12; x = +6. Значит степень окисления хрома в дихромате калия равна (+6). Это верный ответ. |
| Ответ | Вариант (б) |











