Степень окисления в N2O5
Общие сведения об оксиде азота (V) и степени окисления в N2O5
При нагревании возгоняется и плавится, при комнатной температуре разлагается за 10 часов. В твердом состоянии имеет ионное строение (показано на рис. 1) (NO2+) (NO3—) – нитрат нитроила. Брутто-формула – N2O5. Молярная масса равна 108,01 г/моль. Температура плавление 41oC.
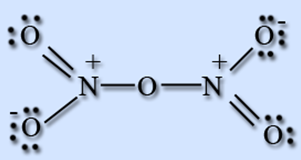
Рис. 1. Строение молекулы оксида азота (V).
Проявляет кислотные свойства, реагирует с водой, щелочами, гидратом аммиака. Очень сильный окислитель.
N2O5, степени окисления элементов в нем
Чтобы определить степени окисления элементов, входящих в состав оксида азота (V), сначала необходимо разобраться с тем, для каких элементов эта величина точно известна.
Степень окисления кислорода в оксидах всегда равна ( — 2). Для нахождения степени окисления азота примем её значение за «х» и определим его при помощи уравнения электронейтральности:
2×х + 5× (-2)= 0;
2х – 10 = 0;
2х = 10;
x = +5.
Степень окисления азота в оксиде азота (V) равна (+5):
N+52O-25.
Примеры решения задач
| Задание | Установите соответствие между схемами превращения веществ и изменение степени окисления серы:
|
|||||||||||
| Ответ | Будем поочередно определять степень окисления серы в каждой из предложенных схем превращений, а затем выберем верный вариант ответа.
|
| Задание | В соединениях NH4Cl, LiClO4, Cl2O степень окисления хлора соответственно равна:
а) -1, +7, +3; б) +3, +7, -1; в) -1, +5, -3; г) -1, +7, +1. |
| Решение |
Для того, чтобы дать правильный ответ на поставленный вопрос будем поочередно определять степень окисления хлора в каждом из предложенных соединений с помощью уравнения электронейтральности. а) Степень окисления азота в ионе аммония равна (-3), а водорода — (+1). Примем за «х» значение степени окисления хлора: (-3) + 4×1 + х = 0; x +1 = 0; x = — 1. б) Степень окисления лития всегда равна (+1). Степень окисления кислорода в данном случае равна (-2). Примем за «х» значение степени окисления хлора: 1 + х + 4×(-2) = 0; x -7 = 0; x = +7. в) Степень окисления кислорода в оксидах всегда равна (-2). Примем за «х» значение степени окисления хлора: 2×х + (-2) = 0; 2х = 2; x = +1. Следовательно, последовательность степеней окисления хлора в соединениях будет следующей: -1, +7, +1. |
| Ответ | Вариант (г) |











