Степень окисления в CS2
Общие сведения о сероуглероде и степени окисления в CS2
Брутто- формула – CS2 (строение молекулы изображено на рис. 1). Молярная масса сероуглерода равна 76,14 г/моль. Температура кипения – 46,24oC.
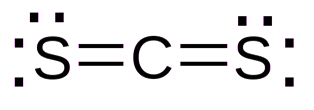
Рис. 1. Строение молекулы сероуглерода.
Мало смешивается с водой, неограниченно смешивается с полярными органическими растворителями. Хорошо растворяет бром, серу и белый фосфор. Реакционноспособное вещество. Легко воспламеняется на воздухе. Гидролизуется водяным паром. В ОВР проявляет свойства восстановителя.
CS2, степени окисления элементов в нем
Чтобы определить степени окисления элементов, входящих в состав сероуглерода, сначала необходимо разобраться с тем, для каких элементов эта величина точно известна.
Сероуглерод представляет собой кислотный ангидрид. Известно, что степень окисления углерода в данном соединении равна (+4). Для нахождения степени окисления серы примем её значение за «х» и определим его при помощи уравнения электронейтральности:
(+4) + 2×х = 0;
4 + 2х = 0;
2х = – 4;
x = -2.
Степень окисления серы в сероуглероде равна (-2):
C+4S-22.
Примеры решения задач
| Задание | Установите соответствие между формулой вещества и степенью окисления азота в нем.
|
||||||||||||
| Ответ | Будем поочередно определять степень окисления азота в каждом из соединений, а затем сопоставим с предложенными вариантами ответа.
а) Фторид нитрозила – NOF представляет собой оксид-фторид азота. Как известно, степень окисления кислорода в составе оксидов всегда равна (-2). Степень окисления фтора всегда равна (-1).Для нахождения степени окисления азота примем её значение за «х» и определим его при помощи уравнения электронейтральности: x + (-2) + (-1) = 0; x — 2-1 = 0; x — 3= 0; x = +3. Значит степень окисления азота во фториде нитрозиларавна (+3). Вариант 4. б) Диметиламин — (CH3)2NH представляет собой аминопроизводное метана. Аминогруппа имеет состав NH2— и получена от аммиака, в котором степень окисления азота равна (-3). Значит степень окисления азота в диметаламинеравна ( — 3). Вариант 1. в) Бромид аммония — NH4Br это производное аммиака, степень окисления азота в котором равна (-3). Значит степень окисления азота в бромиде аммония равна ( — 3). Вариант 1. г) Гидразин — N2H4 представляет собой гидрид азота. Как известно, степень окисления водорода в гидридах неметаллов всегда равна (+1). Для нахождения степени окисления азота примем её значение за «х» и определим его при помощи уравнения электронейтральности: 2×х + 4× (+1)= 0; 2х + 4 = 0; 2х = -4; x = -2. Значит степень окисления азота в гидразине равна (-2). Вариант 2. |
| Задание | В каком соединении степень окисления хлора равна (+5): а) Ca(ClO2)2; б) Cl2O7; в) NaClO4; г) KClO3. |
| Решение | Будем поочередно определять степень окисления хлора в каждом из соединений, а выберем то, в котором его степень окисления равна (+5).
а) Хлорная известь — Ca(OCl)2. Степень окисления кальция постоянна и равна номеру группы Периодической системы Д.И. Менделеева, в которой он расположен со знаком плюс (кальций – металл), т.е. (+2). Степень окисления кислорода в составе кислот, а, следовательно, и их остатков равна (-2). Для нахождения степени окисления хлора примем её значение за «х» и определим его при помощи уравнения электронейтральности: (+2) + 2× (-2) + 2×х = 0; 2 — 4 + 2х = 0; 2х — 2= 0; 2х = 2; x = -1. Степень окисления хлора равна (-1). б) Оксид хлора (VII) — Cl2O7.Степень окисления кислорода в оксидах всегда равна ( — 2). Для нахождения степени окисления хлора примем её значение за «х» и определим его при помощи уравнения электронейтральности: 2×х + 7× (-2)= 0; 2х – 14 = 0; 2х = 14; x = +7. Степень окисления хлора равна (+7). в) Степени окисления натрия постоянна и равна номеру группы Периодической системы Д.И. Менделеева, в которой он расположен, со знаком плюс (натрий – металл), т.е. (+1). Степень окисления кислорода в составе кислот, а, значит и в их остатках равна (-2). Для нахождения степени окисления хлора примем её значение за «х» и определим его при помощи уравнения электронейтральности: (+1) + х + 4× (-2)= 0; 1 + х – 8 = 0; x — 7= 0; x = +7. Степень окисления хлора равна (+7). г) Степени окисления калия постоянна и равна номеру группы Периодической системы Д.И. Менделеева, в которой он расположен, со знаком плюс (калий – металл), т.е. (+1). Степень окисления кислорода в составе кислот, а, значит и в их остатках равна (-2). Для нахождения степени окисления хлора примем её значение за «х» и определим его при помощи уравнения электронейтральности: (+1) + х + 3× (-2)= 0; 1 + х – 6= 0; x — 5= 0; x = +5. Степень окисления хлора равна (+5). Это верный ответ. |
| Ответ | Вариант (г) |











