Степень окисления в CH4
Общие сведения о метане и степени окисления в CH4
Брутто-формула – CH4. Молярная масса равна – 16/моль.
Молекула метана имеет тетраэдрическую форму (строение представлено на рис. 1): в гибридизацию вступают все валентные электроны углерода, следовательно, атом углерода находится в sp3-гибридизации.
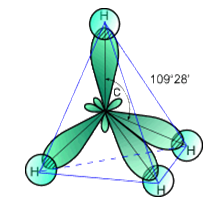
Рис. 1. Строение молекулы метана.
Растворим в этаноле, эфире, углеводородах и мало растворим в воде (45 мл в 1 л воды при 20oС).
CH4, степени окисления элементов в нем
Чтобы определить степени окисления элементов, входящих в состав метана, сначала необходимо разобраться с тем, для каких элементов эта величина точно известна.
Метан – это соединение углерода с водородом, которое по сути представляет собой гидрид углерода. Как известно, степень окисления водорода в гидридах неметаллов равна (+1). Для нахождения степени окисления углерода примем её значение за «х» и определим его при помощи уравнения электронейтральности:
x + 4×(+1) = 0;
x +4 = 0;
x = -4.
Значит степень окисления углерода в метане равна (-4):
С—4H+14.
Примеры решения задач
| Задание | Укажите соответствие между изменением степени окисления хлора в реакции и формулами веществ, которые вступают в эту реакцию.
|
||||||||||||
| Ответ | Чтобы дать правильный ответ на поставленный вопрос запишем продукты всех указанных реакций и определим, как изменилась в ходе взаимодействия степень окисления хлора.
4KCl+5O3 = 2KCl+7O4 + KCl-1 (Cl+5 → Cl-1); 3Cl02 + 6NaOH = 5NaCl-1 + NaCl+5O3 + 3H2O (Cl0 → Cl-1иCl0 → Cl+5); 2KCl-1 + H2SO4 = K2SO4 + HCl-1 (степень окисления хлора не изменилась); 2HCl-1 + F2 = 2HF + Cl02 (Cl-1 → Cl0); KCl-1 + O2 = KCl+5O3 (среди предложенных вариантов нет такого ответа); 2KClO4 + H2SO4 = K2SO4 + 2HClO4 (степень окисления хлора не изменилась). |
| Задание | Определите степени окисления азота в следующих соединениях: а) N2; б) HNO3; в) Ba(NO2)2. |
| Ответ | а)В соединениях с неполярными связями степень окисления элементов равна нулю. Это означает, что степень окисления азота в его двухатомной молекуле равна нулю: N02.
б) Степени окисления водорода и кислорода в составе неорганических кислот всегда равны (+1) и (-2) соответственно. Для нахождения степени окисления азота примем её значение за «х» и определим его при помощи уравнения электронейтральности: (+1) + х + 3×(-2) = 0; 1 + х — 6 = 0; x — 5 = 0; x = +5. Степень окисления азота в азотной кислоте равна (+5): HN+5O3. в)Барий проявляет постоянную степень окисления, совпадающую с номером группы в Периодической системе Д.И. Менделеева, в которой он расположен, т.е. равна (+2) (барий – металл). Степень окисления кислорода в составе неорганических кислот и их остатков всегда равна (-2). Для нахождения степени окисления азота примем её значение за «х» и определим его при помощи уравнения электронейтральности: (+2) + 2×х + 4×(-2) = 0; 2 + 2х — 8 = 0; 2х -6 = 0; 2х = 6; x = +3. Степень окисления азота в нитрите бария равна (+3):Ba(N+3O2)2. |











