Степень окисления в CCl4
Общие сведения о четыреххлористом углероде и степени окисления в CCl4
Плотность – 1,5954 г/см3. Брутто-формула – CCl4 (строение молекулы изображено на рис. 1). Молярная масса равна 153,82 г/моль.
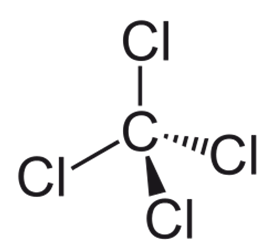
Рис. 1. Строение молекулы тетрахлорметана.
Нерастворим в воде, однако при нагревании в этом тетрахлорметана в этом растворителе до температуры равной 250oC подвергается гидролизу. Смешивается со многими органическими растворителями.
CCl4, степени окисления элементов в нем
Чтобы определить степени окисления элементов, входящих в состав тетрахлорметана, сначала необходимо разобраться с тем, для каких элементов эта величина точно известна.
Тетрахлор метан – это галогенпроизводное метана, в котором все атомы водорода были замещены на атомы хлора. Это означает, что степени окисления углерода в метане и тетрахлорметане равны.
Метан – это соединение углерода с водородом, которое по сути представляет собой гидрид углерода. Как известно, степень окисления водорода в гидридах неметаллов равна (+1). Для нахождения степени окисления углерода примем её значение за «х» и определим его при помощи уравнения электронейтральности:
x + 4×(+1) = 0;
x +4 = 0;
x = -4.
Степень окисления углерода в метане равна (-4), значит и в тетрахлорметане имеет такое же значение:
С—4Cl+14.
Примеры решения задач
| Задание | Установите соответствие между формулой соли и степенью окисления углерода в ней.
|
||||||||||||
| Ответ | Определим степень окисления углерода в каждом из предложенных соединений и сопоставим с возможными вариантами ответа.
а) Карбонат калия — K2CO3. Степень окисления калия постоянна и равна номеру группы Периодической системы Д.И. Менделеева, в которой он расположен со знаком плюс (калий – металл), т.е. (+1). Степень окисления кислорода в составе кислот, а, следовательно, и их остатков равна (-2). Для нахождения степени окисления углерода примем её значение за «х» и определим его при помощи уравнения электронейтральности: 2×(+1) + х + 3× (-2) = 0; 2 + х — 6 = 0; x – 4 = 0; x = +4. Степень окисления углерода в карбонате калия равна (+4). Вариант 6. б) Гидрокарбонат кальция — Ca(HCO3)2. Степень окисления кальция постоянна и равна номеру группы Периодической системы Д.И. Менделеева, в которой он расположен со знаком плюс (кальций – металл), т.е. (+2). Степени окисления кислорода и водорода в составе кислот, а, следовательно, и их остатков равны (-2) и (+1) соответственно. Для нахождения степени окисления углерода примем её значение за «х» и определим его при помощи уравнения электронейтральности: (+2) + 2×(+1) + 2×х + 6× (-2) = 0; 2 + 2 + 2х -12= 0; 2х — 8= 0; 2х = 8; x = +4. Степень окисления углерода в гидрокарбонате кальция равна (+4). Вариант 6. в) Формиат натрия — HCOONa. Степень окисления натрия постоянна и равна номеру группы Периодической системы Д.И. Менделеева, в которой он расположен со знаком плюс (натрий – металл), т.е. (+1). Степени окисления кислорода и водорода в составе органических кислот всегда равны (-2) и (+1) соответственно. Для нахождения степени окисления углерода примем её значение за «х» и определим его при помощи уравнения электронейтральности: (+1) + х + 2× (-2) + (+1)=0; 1 + х – 4 + 1 = 0; x – 2 = 0; x = +2. Степень окисления углерода в формиате натрия равна (+2). Вариант 3. г) Гидрооксалат натрия — NaHC2O4. Степень окисления натрия постоянна и равна номеру группы Периодической системы Д.И. Менделеева, в которой он расположен со знаком плюс (натрий – металл), т.е. (+1). Степени окисления кислорода и водорода в составе органических кислот всегда равны (-2) и (+1) соответственно. Для нахождения степени окисления углерода примем её значение за «х» и определим его при помощи уравнения электронейтральности: (+1) + (+1) + 2×х + 4× (-2)= 0; 1 + 1 + 2х – 8 = 0; 2х – 6 = 0; 2х = 6; x = +3. Степень окисления углерода в гидрооксалате натрия равна (+2). Вариант 5. |
| Задание | Степень окисления (+3) атом хлора имеет в соединении: а) ClO3; б) Cl2O7; в) Ba(ClO2)2; г) KClO3. |
| Решение | Будем поочередно определять степень окисления хлора в каждом из предложенных соединений, а затем выберем то, в котором это значение равно (+3).
а) Степень окисления кислорода в оксидах всегда равна ( — 2). Для нахождения степени окисления хлора примем её значение за «х» и определим его при помощи уравнения электронейтральности: x + 3× (-2)= 0; x – 6 = 0; x = +6. Степень окисления хлора равна (+6). Это неверный ответ. б) Аналогичным образом определяем степень окисления хлора в данном оксиде: 2×х + 7×(-2)= 0; 2х – 14 = 0; 2х = 14; x = +7. Степень окисления хлора равна (+7). Это неверный ответ. в) Степень окисления бария постоянна и равна номеру группы Периодической системы Д.И. Менделеева, в которой он расположен со знаком плюс (барий – металл), т.е. (+2). Степень окисления кислорода в составе кислот, а, следовательно, и их остатков равна (-2). Для нахождения степени окисления хлора примем её значение за «х» и определим его при помощи уравнения электронейтральности: (+2) + 2×х + 4× (-2) = 0; 2 + 2х — 8 = 0; 2х – 6 = 0; 2х = 6; x = +3. Степень окисления углерода равна (+3). Это верный ответ. |
| Ответ | Вариант (в) |











