Метиловый спирт
Характеристики и физические свойства метилового спирта
Представляет собой бесцветную горючую жидкость со спиртовым запахом. Смешивается с водой в любых отношениях, чрезвычайно ядовит. Принятие внутрь даже нескольких капель вызывает тяжелое отравление, потерю зрения, возможен смертельный исход.
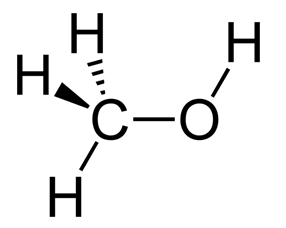
Рис. 1. Строение молекулы метилового спирта.
Основные характеристики метилового спирта приведены в таблице ниже:
|
Молекулярная формула |
CH3OH |
|
Молярная масса, г/моль |
32 |
|
Плотность, г/см3 |
0,7918 |
|
Температура плавления, oС |
-97 |
|
Температура кипения, oС |
64,7 |
Получение метилового спирта
Метиловый спирт можно получить следующими способами:
— гидролиз моногалогеналканов водными растворами щелочей
CH3Br + NaOHaq→CH3OH + NaBr (t0);
— гидрирование муравьиного альдегида
H-C(O)H + H2→CH3OH (kat = Ni, t0);
— каталитическое окисление метана
2CH4 + O2→ 2CH3OH (p, t0).
Химические свойства метилового спирта
Для метилового спирта характерны следующие химические свойства
- взаимодействие с активнымиметаллами
2CH3OH + 2Na → 2CH3ONa + H2↑.
- взаимодействие с органическими и кислородсодержащими неорганическими кислотами
CH3OH + CH3COOH ↔CH3-O-C(O)-CH3 + H2O (H2SO4 (conc), t0);
CH3OH + HONO2↔CH3ONO2 + H2O (H2SO4 (conc), t0).
- взаимодействие с галогеноводородами
CH3OH + HCl→CH3Cl + H2O (ZnCl2, t0).
- взаимодействие с тригалогенидамифосфора
3CH3OH + PBr3→ 3CH3Br + H3PO3.
- взаимодействие с аммиаком
CH3OH + NH3→CH3NH2 + H2O (Al2O3, t0 = 300).
- окисление
CH3OH + 2[O] →HCOOH + H2O (kat, t0).
Применение метилового спирта
Метиловый спирт широко используется как растворитель и как исходное сырье в органическом синтезе.
Примеры решения задач
| Задание | Какая масса метанола образуется при гидролизе метилацетата, массой 10 г? |
| Решение | Запишем уравнение гидролиза метилового эфира уксусной кислоты:
CH3— C(O)O- CH3 +H2O = CH3COOH + CH3OH. Определим количество вещества метилацетата, используя значение его массы из условия задачи (молярная масса – 84 г/моль): n = m/ M; n (CH3-C(O)O-CH3) = m (CH3-C(O)O-CH3)/ M (CH3-C(O)O-CH3) = 10/84 = 0,12 моль. По уравнению n (CH3— C(O)O- CH3) = n (CH3OH) =0,12 моль. Рассчитаем массу метанола (молярная масса – 32 г/моль): m= n× M; m(CH3OH)= n(CH3OH)× M(CH3OH) = 0,12×32 = 3,84 г. |
| Ответ | Масса метанола, образовавшегося в реакции равна 3,84 г. |
| Задание | В метанол поместили металлический натрий. К реакционной смеси добавили бромэтан. Какое вещество при этом образуется. Составьте уравнения протекающих реакций. |
| Ответ | При действии металлического натрия на метанол образуется соединение подобное соли, называемое алкоголятом:
2CH3-OH + 2Na → 2CH3-ONa + H2. Последующее добавление к реакционной смеси бромэтана привело к образованию простого эфира (метилэтилового) [реакция Вильямсона]: CH3-ONa + C2H5Br → CH3-O-C2H5 + NaBr. |











