Карбоновые кислоты
Характеристики и физические свойства карбоновых кислот
Первые три члена гомологического ряда карбоновых кислот, включая пропионовую кислоту, — жидкости, имеющие резкий запах, хорошо растворимые в воде. Следующие гомологи, начиная с масляной кислоты, — также жидкости, обладающие резким неприятным запахом, но плохо растворимые в воде. Высшие кислоты, с числом атомов углерода 10 и более, представляют собой твердые вещества, без запаха, нерастворимые в воде. В целом, в ряду гомологов с увеличением молекулярной массы уменьшается растворимость в воде, уменьшается плотность и возрастает температура кипения (табл. 1).
Таблица 1. Гомологический ряд карбоновых кислот.
|
Формула |
Название |
Плотность, г/см3 |
Температура кипения, oС |
|
H-COOH |
Муравьиная (метановая) |
1,220 |
100,7 |
|
CH3-COOH |
Уксусная (этановая) |
1,049 |
118,1 |
|
CH3-CH2-COOH |
Пропионовая (пропановая) |
0,992 |
141,4 |
|
CH3-CH2-CH2-COOH |
Масляная (бутановая) |
0,964 |
163,5 |
|
CH3-(CH2)3-COOH |
Валериановая (пентановая) |
0,939 |
186,4 |
|
CH3-(CH2)4-COOH |
Капроновая (гексановая) |
0,929 |
205,3 |
|
CH3-(CH2)5-COOH |
Энантовая (гептановая) |
0,910 |
222 |
Получение карбоновых кислот
Карбоновые кислоты получают окислением предельных углеводородов, спиртов, альдегидов. Например, уксусную кислоту – окислением этанола раствором перманганата калия в кислой среде при нагревании:
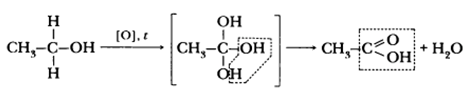
Химические свойства карбоновых кислот
Химические свойства карбоновых кислот обусловлены в первую очередь особенностями их строения. Так, растворимые в воде кислоты способны диссоциировать на ионы:
R-COOH↔R-COO— + H+.
Благодаря наличию в воде иона H+ они имеют кислый вкус, способны менять окраску индикаторов и проводить электрический ток. В водном растворе эти кислоты – слабые электролиты.
Карбоновые кислоты обладают химическими свойствами, характерными для растворов неорганических кислот, т.е. взаимодействуют с металлами (1), их оксидами (2), гидроксидами (3) и слабыми солями (4):
2CH3-COOh + Zn → (CH3COO)2Zn + H2↑ (1);
2CH3-COOH + CuO→ (CH3COO)2Cu + H2O (2);
R-COOH + KOH → R-COOK + H2O (3);
2CH3-COOH + NaHCO3→ CH3COONa + H2O + CO2↑ (4).
Специфическое свойство предельных, а также непредельных карбоновых кислот, проявляемое за счет функциональной группы, — взаимодействие со спиртами.
Карбоновые кислоты взаимодействуют со спиртами при нагревании и в присутствии концентрированной серной кислоты. Например, если к уксусной кислоте прилить этиловый спирт и немного серной кислоты, то при нагревании появляется запах этилового эфира уксусной кислоты (этилацетата):
CH3-COOH + C2H5OH ↔CH3-C(O)-O-C2H5 + H2O.
Специфическое свойство предельных карбоновых кислот, проявляемое за счет радикала, — реакция галогенирования (хлорирования).
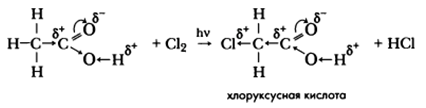
Применение карбоновых кислот
Карбоновые кислоты служат исходным сырьем для получения кетонов, галогенангидридов, виниловых эфиров и других важных классов органических соединений.
Муравьиная кислота широко применяется для получения сложных эфиров, используемых в парфюмерии, в кожевенном деле (дубление кож), текстильной промышленности (как протрава при крашении), в качестве растворителя и консерванта.
Водный раствор (70-80%-ной) уксусной кислоты называется уксусной эссенцией, а 3-9%-ный водный раствор – столовым уксусом. Эссенция нередко используется для получения уксуса в домашних условиях путем разведения.
Примеры решения задач
| Задание | С помощью каких химических реакций можно осуществить следующие превращения:
а) CH4→ CH3Cl → CH3OH → HCHO → HCOOH → HCOOK. Напишите уравнения реакций, укажите условия их протекания. |
| Ответ | а) Хлорирование метана на свету приводит к получению хлорметана:
CH4 + Cl2→CH3Cl + HCl. Галогенпроизводные алканов подвергаются гидролизу в водной или щелочной среде с образованием спиртов: CH3Cl + NaOH→CH3OH + NaCl. В результате окисления первичных спиртов, например, дихроматом калия в кислой среде в присутствии катализатора (Cu, CuO, Pt, Ag) образуются альдегиды: CH3OH+ [O] →HCHO. Альдегиды легко окисляются до соответствующих карбоновых кислот, например, перманганатом калия: HCHO + [O] →HCOOH. Карбоновые кислоты, проявляют все свойства, присущие слабым минеральным кислотам, т.е. способны взаимодействовать с активными металлами с образованием солей: 2HCOOH+ 2K→2HCOOK + H2↑. |
| Задание | Напишите уравнения реакций между следующими веществами: а) 2-метилпропановой кислотой и хлором; б) уксусной кислотой и пропанолом-2; в) акриловой кислотой и бромной водой; г) 2-метилбутановой кислотой и хлоридом фосфора (V). Укажите условия протекания реакций. |
| Ответ | а) в результате реакции взаимодействия между 2-метилпропановой кислотой и хлором происходит замещение атома водорода в углеводородном радикале, находящемся в a-положение; образуется 2-метил-2-хлорпропановая кислота
H3C-C(CH3)H-COOH + Cl2→ H3C-C(CH3)Cl-COOH + HCl (kat = P). б) в результате реакции взаимодействия между уксусной кислотой и пропанолом-2 происходит образование сложного эфира – изопропиловый эфир уксусной кислоты. CH3-COOH + CH3-C(OH)H-CH3→ CH3-C(O)-O-C(CH3)-CH3. в) в результате реакции взаимодействия между акриловой кислотой и бромной водой присоединение галогена по месту двойной связи в соответствии с правилом Марковникова; образуется 2,3-дибромпропановая кислота CH2=CH-COOH + Br2→ CH2Br-CHBr-COOH г) в результате реакции взаимодействия между 2-метилбутановой кислотой и хлоридом фосфора (V) образуется соответствующий хлорангидрид CH3-CH2-C(CH3)H-COOH + PCl5→CH3-CH2-C(CH3)H-COOCl + POCl3 + HCl. |











