Бензол
Характеристики и физические свойства бензола
Ароматические свойства бензола, определяемые особенностями его структуры, выражаются в относительной устойчивости бензольного ядра, несмотря на непредельность бензола по составу. Так, в отличие от непредельных соединений с этиленовыми двойными связями, бензол устойчив к действию окислителей.
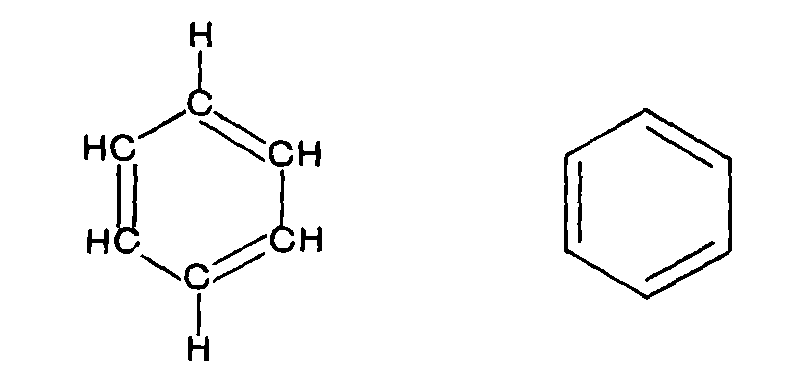
Рис. 1. Строение молекулы бензола по Кекуле.
Получение бензола
К основным способам получения бензола относятся:
— дегидроциклизация гексана (катализаторы – Pt, Cr3O2)
CH3 –(CH2)4-CH3 → C6H6 + 4H2↑ (toC, p, kat = Cr2O3);
— дегидрированиециклогексана
C6H12 → C6H6 + 3H2↑ (toC, kat = Pt, Ni);
— тримеризация ацетилена (реакция протекает при нагревании до 600oС, катализатор – активированный уголь)
3HC≡CH → C6H6 (t = 600oC, kat = Сactiv).
Химические свойства бензола
Для бензола характерны реакции замещения, протекающие по электрофильному механизму:
-галогенирование (бензол взаимодействует с хлором и бромом в присутствии катализаторов – безводных AlCl3, FeCl3, AlBr3)
C6H6 + Cl2 = C6H5-Cl + HCl;
— нитрование (бензол легко реагирует с нитрующей смесью – смесь концентрированных азотной и серной кислот)
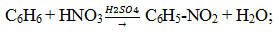
— алкилирование по Фридею-Крафтсу
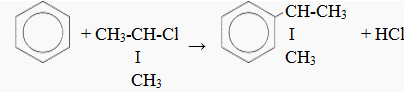
— алкилирование алкенами
C6H6 + CH2=CH-CH3 → C6H5-CH(CH3)2
Реакции присоединения к бензолу приводят к разрушению ароматической системы и протекают только в жестких условиях:
— гидрирование (продукт реакции — циклогексан)
C6H6 + 3H2→ С6H12 (toC, kat = Pt);
— присоединение хлора (протекает под действием УФ-излучения с образованием твердого продукта – гексахлорциклогексана (гексахлорана) – C6H6Cl6)
C6H6+ 6Cl2→C6H6Cl6.
Применение бензола
Бензол широко используется в промышленной органической химии. Практически все соединения, имеющие в своем составе бензольные кольца, получаются из бензола, например, стирол, фенол, анилин, галогензамещенные арены. Бензол используется для синтеза красителей, поверхностно-активных веществ, фармацевтических препаратов.
Примеры решения задач
| Задание | Плотность паров вещества 3,482г/л. Его пиролиз дал 6 г сажи и 5,6 л водорода. Определите формулу этого вещества. |
| Решение | Сажа представляет собой углерод. Найдем количество вещества сажи исходя из условий задачи (молярная масса углерода равна 12 г/моль):
n = m / M; n(C) = m(C) / M(C); n(C) = 6 / 12 = 0,5 моль. Рассчитаем количество вещества водорода: n =V / Vm; n(H2) = V(H2) / Vm; n(H2) = 5,6 / 22,4 = 0,25 моль. Значит, количество вещества одного атома водорода будет равно: n(H) = 2 × 0,25 = 0,5 моль. Обозначим количество атомов углерода в молекуле углеводорода за «х», а количество атомов водорода за «у», тогда соотношение этих атомов в молекуле: х : у = 0,5: 0,5 =1:1. Тогда простейшая формула углеводорода будет выражаться составом СН. Молекулярная масса молекулы состава СН равна: М(СН) = 13 г/моль Найдем молекулярную массу углеводорода исходя из условий задачи: M (CxHy) = ρ×Vm; M (CxHy) = 3,482×22,4 = 78 г/моль. Определим истинную формулу углеводорода: k= M(CxHy)/ М(СН)= 78/13 =6, следовательно, коэффициенты «х» и «у» нужно умножить на 6 и тогда формула углеводорода примет вид C6H6. Это бензол. |
| Ответ | Искомый углеводород имеет состав C6H6. Это бензол. |
| Задание | Рассчитайте количество вещества ацетилена, которое понадобится для получения 400 мл бензола (плотность 0,8 г/мл). |
| Решение | Запишем уравнение реакции получения бензола из ацетилена:
3C2H2 = C6H6. Найдем массу бензола согласно условию задачи: m(C6H6) = ρ×V; m(C6H6) = 0,8×400 = 320 г. Рассчитаем количество вещества бензола (молярная масса – 78 г/моль): n = m / M; n(C6H6) = m(C6H6) / M(C6H6); n(C6H6) = 320/78 = 4,1 моль. Согласно уравнению реакцииn(C6H6) : n(C2H2) = 1:3, т.е. n(C2H2) = 3×n(C6H6); n(C2H2) = 3×4,1 = 12,3 моль. |
| Ответ | Количество вещества ацетилена 12,3 моль. |











