Аминокислоты
Характеристики и физические свойства аминокислот
Аминокислоты представляют собой твердые кристаллические вещества, характеризующиеся высокими температурами плавления и разлагающиеся при нагревании. Они хорошо растворяются в воде. Данные свойства объясняются возможностью существование аминокислот в виде внутренних солей (рис. 1).
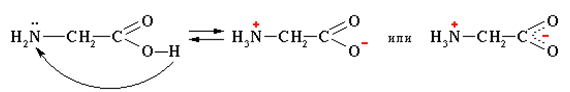
Рис. 1. Внутренняя соль аминоуксусной кислоты.
Получение аминокислот
Исходными соединениями для получения аминокислот часто служат карбоновые кислоты, в молекулу которых вводится аминогруппа. Например, получение их из галогензамещенных кислот
CH3-C(Br)H-COOH + 2NH3→CH3-C(NH2)H-COOH + NH4Br.
Кроме этого исходным сырьем для получения аминокислот могут служить альдегиды (1), непредельные кислоты (2) и нитросоединения (3):
CH3-C(O)H + NH3 + HCN → CH3-C(NH2)H-C≡H + H2O;
CH3-C(NH2)H-C≡H + H2O (H+) → CH3-C(NH2)H-COOH + NH3 (1).
CH2=CH-COOH + NH3→ H2N-CH2-CH2-COOH (2);
O2N-C6H4-COOH + [H] →H2N-C6H4-COOH (3).
Химические свойства аминокислот
Аминокислота как гетерофункциональные соединения вступают в большинство реакций, характерных для карбоновых кислот и аминов. Наличие в молекулах аминокислот двух различных функциональных групп приводит к появлению ряда специфических свойств.
Аминокислоты – амфотерные соединения. Они реагируют как с кислотами, так и с основаниями:
NH2–CH2-COOH + HCl→ Cl[NH3–CH2-COOH]
NH2–CH2-COOH + NaOH→ NH2–CH2-COONa + H2O
Водные растворы аминокислот имеют нейтральную, щелочную и кислотную среду в зависимости от количества функциональных групп. Например, глутаминовая кислота образует кислый раствор, поскольку в её составе две карбоксильные группы и одна аминогруппа, а лизин – щелочной раствор, т.к. в её составе одна карбоксильная группа и две аминогруппы.
Две молекулы аминокислоты могут взаимодействовать друг с другом. При этом происходит отщепление молекулы воды и образуется продукт, в котором фрагменты молекулы связаны между собой пептидной связью (-CO-NH-). Например:
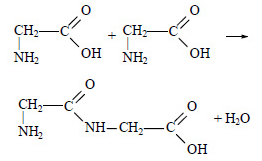
Полученное соединение называют дипептидом. Вещества, построенные из многих остатков аминокислот, называются полипептидами. Пептиды гидролизуются под действием кислот и оснований.
Применение аминокислот
Аминокислоты, необходимые для построения организма, как человек, так и животные получают из белков пищи.
γ-Аминомасляная кислота используется в медицине (аминалон / гаммалон) при психических заболеваниях; на её основе создан целый ряд ноотропных препаратов, т.е. оказывающих влияние на процессы мышления.
ε-Аминокапроновая кислота также используется в медицине (кровоостанавливающее средство), а кроме того представляет собой крупнотоннажный промышленный продукт, использующийся для получения синтетического полиамидного волокна – капрона.
Антраниловая кислота используется для синтеза красителей, например синего индиго, а также участвует в биосинтезе гетероциклических соединений.
Примеры решения задач
| Задание | Напишите уравнения реакций аланина с: а) гидроксидом натрия; б) гидроксидом аммония; в) соляной кислотой. За счет каких групп внутренняя соль проявляет кислотные и основные свойства? |
| Ответ | Аминокислоты часто изображают как соединения, содержащие аминогруппу и карбоксильную группу, однако с такой структурой не согласуются некоторые их физические и химические свойства. Строение аминокислот соответствует биполярному иону:
H3N+-CH(R)-COO—. Запишем формулу аланина как внутренней соли: H3N+-CH(CH3)-COO—. Исходя из этой структурной формулы, напишем уравнения реакций: а) H3N+-CH(CH3)-COO— + NaOH = H2N-CH(CH3)-COONa + H2O; б) H3N+-CH(CH3)-COO— + NH3×H2O = H2N-CH(CH3)-COONH4 + H2O; в) H3N+-CH(CH3)-COO— + HCl = [H3N+-CH(CH3)-COOH]Cl—. Внутренняя соль аминокислоты реагирует с основаниями как кислота, с кислотами – как основание. Кислотная группа – N+H3, основная – COO—. |
| Задание | При действии на раствор 9,63 г неизвестной моноаминокарбоновой кислоты избытком азотистой кислоты было получено 2,01 л азота при 748 мм. рт. ст. и 20oС. Определите молекулярную формулу этого соединения. Может ли эта кислоты быть одной из природных аминокислот? Если да, то какая это кислота? В состав молекулы этой кислоты не входит бензольное кольцо. |
| Решение | Напишем уравнение реакции:
H2NCxH2xCOOH + HONO = HO-CxH2x-COOH + N2 + H2O. Найдем количество вещества азота при н.у., применяя уравнение Клапейрона-Менделеева. Для этого температуру и давление выражаем в единицах СИ: T = 273 + 20 = 293 K; P = 101,325 × 748 / 760 = 99,7 кПа; n= pV / RT; n(N2) = 99,7 × 2,01 / 8,31 × 293 = 0,082 моль. По уравнению реакции находим количество вещества аминокислоты и её молярную массу. По уравнению n(H2NCxH2xCOOH) = n(N2) = 0,082 моль. M(H2NCxH2xCOOH) = 9,63 / 0,082 = 117 г/моль. Определим аминокислоту. Составим уравнение и найдем x: 14x + 16 + 45 = 117; x = 4; H2NC4H8COOH. Из природных кислот такому составу может отвечать валин. |
| Ответ | Эта аминокислота — валин. |











